题目内容
19.在一定条件下,甲和乙反应生成丙的微观示意图如下,则下列说法中错误的是( )
| A. | 该反应属于化合反应 | |
| B. | .反应前后分子的个数没有改变 | |
| C. | 一个X分子中含有三个原子 | |
| D. | 参加反应的甲、乙两种物质质量比为7:4 |
分析 根据在一定条件下,甲和乙反应生成丙的微观示意图和质量守恒定律,分析反应物、生成物写出反应的化学方程式,据其意义分析判断
解答 解:由一定条件下,甲和乙反应生成丙的微观示意图和质量守恒定律可知,该反应是一氧化碳燃烧生成了二氧化碳,方程式是:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2
A、该反应由两种物质生成了一种物质,属于化合反应,故A正确;
B、由方程式可知,每3个分子变化成了2个分子,反应前后分子的个数发生了改变,故B错误;
C、一个X分子中含有三个原子,故C正确;
D、由方程式可知,参加反应的甲、乙两种物质质量比为(28×2):32=7:4,故D正确.
故选B.
点评 解答本题比较简便的方法是根据微观示意图写出反应的化学方程式,根据方程式的意义分析解答.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
9.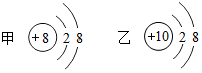 甲、乙是两种粒子的结构示意图,下列说法正确的是( )
甲、乙是两种粒子的结构示意图,下列说法正确的是( )
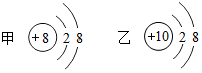 甲、乙是两种粒子的结构示意图,下列说法正确的是( )
甲、乙是两种粒子的结构示意图,下列说法正确的是( )| A. | 甲是阳离子 | B. | 甲、乙化学性质相同 | ||
| C. | 甲、乙属于不同种元素 | D. | 甲、乙都属于金属元素 |
10.下列说法正确的是( )
| A. | 煤、石油、天然气是当今最重要的三大矿物燃料,是取之不尽的 | |
| B. | 煤是一种复杂的混合物,主要含有碳、氢两种元素 | |
| C. | 石油主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素 | |
| D. | 煤和石油都是由古代植物遗体埋在地层下或在地壳中经过一系列非常复杂的变化而形成的 |
14.咱们学校化学兴趣小组的同学,对实验室制备氧气的若干问题进行如下探究:
【探究一】为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
(1)写出本实验中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;测量O2体积的装置是c (选填下图l中的装置编号).

(2)由实验I、II、III可知:影响双氧水分解速率的因素是:双氧水的浓度.
【探究二】B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.于是他们用天平称量0.2g氧化铜,取5%过氧化氢溶液5mL于试管中,进行如图2实验:

(1)填写如表:
(2)步骤①的目的是与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化,步骤④对应的实验操作是过滤,步骤⑦是证明氧化铜的化学性质在反应前后没有改变.
【探究一】为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

(2)由实验I、II、III可知:影响双氧水分解速率的因素是:双氧水的浓度.
【探究二】B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.于是他们用天平称量0.2g氧化铜,取5%过氧化氢溶液5mL于试管中,进行如图2实验:

(1)填写如表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| 有大量气泡产生. | 称得氧化铜质量为0.2g. | 将固体加入盛有5mL 5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象. | 在过氧化氢溶液的分解实验中,氧化铜也能作催化剂. |
4.燃烧与我们的生活和社会的发展有着密切的联系.某兴趣小组活动中,同学们按如图1所示装置对“可燃物燃烧的条件”进行探究.

(1)图1中发生反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,该实验装置的缺点是反应生成的白烟会污染空气.
(2)同学们按图2所示装置对该实验进行改进.
(3)小于指出图2装置仍有不足之处,并设计了如图3所示装置,其中气球的作用是避免橡皮塞因试管内气体热膨胀而松动或飞出.
(4)小组同学又做了如图4所示实验.
①写出A试管中发生反应的现象:白磷剧烈燃烧,产生大量的白烟,放出热量.
②待试管冷却至室温,在水中取下胶塞,试管中液面上升(如图B所示),试管内液面上升的原因是白磷燃烧消耗氧气,生成固体,使试管内气体压强减小,小于外界大气压,所以试管内液面上升.

(1)图1中发生反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,该实验装置的缺点是反应生成的白烟会污染空气.
(2)同学们按图2所示装置对该实验进行改进.
| 实验现象 | 解释 |
| a试管中白磷燃烧,热水中白磷没有燃烧 | 原因是热水中的白磷没有与氧气接触 |
| b试管中红磷没有燃烧 | 原因是温度未达到红磷的着火点 |
(4)小组同学又做了如图4所示实验.
①写出A试管中发生反应的现象:白磷剧烈燃烧,产生大量的白烟,放出热量.
②待试管冷却至室温,在水中取下胶塞,试管中液面上升(如图B所示),试管内液面上升的原因是白磷燃烧消耗氧气,生成固体,使试管内气体压强减小,小于外界大气压,所以试管内液面上升.
11.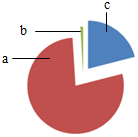 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )
 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
 课题式课堂教学是探究学习的一种方式,其基本教学模式为:提出课题→确定研究方案→解决问题→总结和评价.图1是关于《一氧化碳的化学性质》的课题式课堂教学中,在解决问题阶段甲同学设计的证明CO具有还原性的实验装置,装置气密性良好.
课题式课堂教学是探究学习的一种方式,其基本教学模式为:提出课题→确定研究方案→解决问题→总结和评价.图1是关于《一氧化碳的化学性质》的课题式课堂教学中,在解决问题阶段甲同学设计的证明CO具有还原性的实验装置,装置气密性良好.