题目内容
17.俄国化学家门捷列夫制作出了元素周表,为人类研究化学做出了巨大贡献,下面有关元素周期表有叙述正确的是( )| A. | 纵行不周期,横行为族 | |
| B. | 原子序数与元素的原子核外电子数相等 | |
| C. | 原子序数与元素相对原子质量的数值相等 | |
| D. | 元素周期表是根据原子核内中子的数目排列的 |
分析 根据元素周期表的组成以及元素周期表的信息来分析解答.
解答 解:A.在元素周期表中,横行为周期,纵行为族,故错误;
B.在原子中,原子序数=核内质子数=核外电子数,故正确;
C.原子序数等于核内质子数,不等于相对原子质量,故错误;
D.元素周期表是根据原子序数(核内质子数)的数目排列的,故错误.
故选B.
点评 掌握元素周期表的组成以及元素周期表的信息是解题的关键.

练习册系列答案
相关题目
7.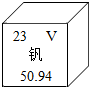 钒被誉为“合金的维生素”,钒元素的相关信息如下,下列有关钒的说法错误的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如下,下列有关钒的说法错误的是( )
 钒被誉为“合金的维生素”,钒元素的相关信息如下,下列有关钒的说法错误的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如下,下列有关钒的说法错误的是( )| A. | 属于金属元素 | B. | 原子核内质子数为23 | ||
| C. | 元素符号为V | D. | 相对原子质量为50.94g |
12.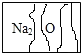 实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.
实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如表实验.
【实验结论】
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
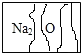 实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.
实验室有了瓶标签受到腐蚀(如图所示)的无色溶液,各学习小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如表实验.
| 实验操作 | 实验现象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液 ②静置后,再去上层清液,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀消失 |
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实验操作 | 实验现象 |
6.将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$ 钠的氧化物 $\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$ 白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH; 2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O 猜想2:Na2O2 猜想3:Na2O和Na2O2
【实验探究一】:
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH
【实验探究二】:
【实验反思】
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl═4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{O_{2}}{→}$ 钠的氧化物 $\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$ 白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH; 2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O 猜想2:Na2O2 猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
【作出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH
【实验探究二】:
| 实验操作 | 实验现象 | 实验结论 |
| 1、取少量白色固体加入足量CaCl2溶液. | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2、过滤、取少量滤液加入 无色酚酞试液 | 试液变红 |
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl═4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
7.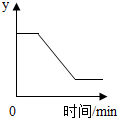 已知:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量随时间的变化趋势,纵坐标表示的是( )
已知:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量随时间的变化趋势,纵坐标表示的是( )
 已知:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量随时间的变化趋势,纵坐标表示的是( )
已知:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量随时间的变化趋势,纵坐标表示的是( )| A. | 固体中氧元素的质量 | B. | 生成氧气的质量 | ||
| C. | 固体中二氧化锰的质量 | D. | 固体中钾元素的质量分数 |
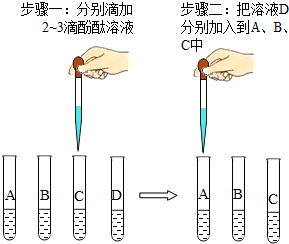 在实验台上有四瓶未贴标签的溶液,已知分別是碳酸钾溶液、氯化钠溶液、氯化钡溶液和稀硫酸.为了鉴别这四种溶液,在老师的指导下,兴趣小组的同学把这四种溶液按A、B、C、D进行编号,分别各取适量作为样品加入到四支试管中,进行了如图所示的探究活动:
在实验台上有四瓶未贴标签的溶液,已知分別是碳酸钾溶液、氯化钠溶液、氯化钡溶液和稀硫酸.为了鉴别这四种溶液,在老师的指导下,兴趣小组的同学把这四种溶液按A、B、C、D进行编号,分别各取适量作为样品加入到四支试管中,进行了如图所示的探究活动: