题目内容
1.若有化学反应4A+B2═2A2B,且A与B元素的相对原子质量之比为1:2,则12gB2完全消耗时生成A2B的质量为( )| A. | 15g | B. | 18g | C. | 24g | D. | 36g |
分析 根据题意,化学反应4A+B2═2A2B,且A与B元素的相对原子质量之比为1:2,据此计算出参加反应的B2和A2B的质量比,由反应的化学方程式,进行分析解答.
解答 解:设生成A2B的质量为x,A与B元素的相对原子质量之比为1:2,则B2与2A2B的质量比为(2×2):【(1×2+2)×2】=4:8.
4A+B2═2A2B
4 8
12g x
$\frac{4}{8}=\frac{12g}{x}$ x=24g.
故选:C.
点评 本题难度不大,灵活运用根据化学方程式的计算方法是正确解答本题的关键.

练习册系列答案
相关题目
11.根据实验规范,图示的操作中正确的是( )
| A. |  滴加液体 | B. |  过滤 过滤 | C. |  液体加热 | D. |  块状固体取用 |
12.下列原子结构示意图中,易失去电子的是( )
| A. |  | B. | 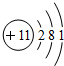 | C. |  | D. |  |
6.下列关于一氧化碳和二氧化碳的说法正确的是( )
| A. | 密度都比空气大 | B. | 都可以用碳和氧气反应得到 | ||
| C. | 都有还原性 | D. | 都能和澄清石灰水发生反应 |
13.为测定氢氧化钠溶液的溶质质量分数,将足量二氧化碳通入20g氢氧化钠溶液中,称量反应后溶液总质量为为21.1g.(1)参加反应的二氧化碳的质量是1.1g.
(2)计算该氢氧化钠溶液中溶质的质量分数.
(2)计算该氢氧化钠溶液中溶质的质量分数.
8.下列方法中,能达到目的是( )
| 选 项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | CO2(CO) | 通入足量的氧气,点燃 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO(CO2) | 循环通过灼热的炭粉 |
| D | KCl(MnO2) | 加足量水溶解后,过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.下列知识整理的内容中,有错误的一组是( )
| A. | 除杂的方法:木炭粉中混有铁粉--用磁铁吸引 | |
| B. | 化学物质中的“三”三大化石燃料--煤、石油、天然气 三种黑色氧化物--氧化铜、二氧化锰、四氧化三铁 | |
| C. | 实验安全注意事项 制取气体--先检查装置的气密性 点燃可燃性气体--先检验气体的纯度 | |
| D. | 化学物质与俗名:二氧化碳--干冰 氢氧化钙--烧碱 |
 如图是制取氧气的装置,某同学用来“碳还原氧化铜”,他的措施是:在酒精灯火焰上罩个铜丝网,目的是集中火焰,提高温度;B中盛一定量的澄清的石灰水,其作用是检验二氧化碳气体;装置的管口连接是:a连接b;写出碳还原氧化铜反应的化学方程式:C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
如图是制取氧气的装置,某同学用来“碳还原氧化铜”,他的措施是:在酒精灯火焰上罩个铜丝网,目的是集中火焰,提高温度;B中盛一定量的澄清的石灰水,其作用是检验二氧化碳气体;装置的管口连接是:a连接b;写出碳还原氧化铜反应的化学方程式:C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.