题目内容
1. (1)等质量的A、B两种物质分别与等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如甲图所示.请回答下列问题:
(1)等质量的A、B两种物质分别与等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如甲图所示.请回答下列问题:①若A、B为Mg、Zn中的一种,则A是镁,反应结束后只有一种金属剩余,则剩余金属为镁.
②若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,反应结束后,则它们消耗的酸相等(填“A多”、“B多”或“相等”).B反应至a点时,所得溶液的溶质为CaCl2、HCl(写化学式).
(2)如乙图所示,A、B、C、D、E分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A是硝酸铜溶液.(“-”相连两物质能发生反应)请回答:
①D的化学式为NaOH,E物质的一种用途:灭火.
②A与B反应的化学方程式Fe+Cu(NO3)2=Fe(NO3)2+Cu,基本反应类型是置换反应.
分析 (1)①根据镁和盐酸反应生成氯化镁和氢气,锌和盐酸反应生成氯化锌和氢气,然后结合金属质量相等和金属活动性顺序进行分析;
②根据粉末状物质和盐酸的接触面积大,反应速率快进行分析;
(2)根据A、B、C、D、E分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,铁会与硝酸铜、稀硫酸反应,硝酸铜会与铁、氢氧化钠反应,二氧化碳会与氢氧化钠反应,稀硫酸会与氢氧化钠、铁反应,氢氧化钠会与稀硫酸、二氧化碳、硝酸铜反应,E会与一种物质反应,所以E是二氧化碳,D就是氢氧化钠,
A是硝酸铜溶液,所以B就是铁,C就是稀硫酸,然后将推出的物质进行验证即可.
解答 解:(1)①镁的活动性比锌强,与酸反应速率快,所以A是镁,24份质量的镁会与73份质量的盐酸反应,65份质量的锌会与73份质量的盐酸反应,所以反应结束后只有一种金属剩余,则剩余金属为镁;
②粉末状物质和盐酸的接触面积大,反应速率快,所以A是碳酸钠,B是碳酸钙,生成44份二氧化碳需要73份质量的盐酸与碳酸钠反应,生成44份质量的二氧化碳需要73份质量的盐酸与碳酸钙反应,所以消耗的酸相等,B反应至a点时,碳酸钙和盐酸没有完全反应,所得溶液的溶质为CaCl2、HCl;
(2)①A、B、C、D、E分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,铁会与硝酸铜、稀硫酸反应,硝酸铜会与铁、氢氧化钠反应,二氧化碳会与氢氧化钠反应,稀硫酸会与氢氧化钠、铁反应,氢氧化钠会与稀硫酸、二氧化碳、硝酸铜反应,E会与一种物质反应,所以E是二氧化碳,D就是氢氧化钠,
A是硝酸铜溶液,所以B就是铁,C就是稀硫酸,经过验证,推导正确,所以D是NaOH,A是二氧化碳,可以用来灭火;
②A与B的反应是铁和硝酸铜反应生成硝酸亚铁和铜,化学方程式为:Fe+Cu(NO3)2=Fe(NO3)2+Cu,该反应属于置换反应.
故答案为:(1)①镁,镁;②相等,CaCl2、HCl;
(2)①NaOH,灭火;②Fe+Cu(NO3)2=Fe(NO3)2+Cu,置换反应.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | NaOH | B. | Na2O | C. | NaH | D. | Na4(OH)4 |
| A. | NH4+ NO3- Na+ Cl- | B. | CO32- K+ Na+ SO42- | ||
| C. | Cu2+ OH- Cl- Ba2+ | D. | Ag+ NO3- Cl- Na+ |
| A. | 糖水 | B. | 金刚石 | C. | 空气 | D. | 石油 |
| A. | 元素 | B. | 分子 | C. | 原子 | D. | 单质 |
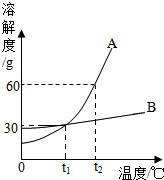 如图是A、B两种物质的溶解度曲线,请回答:
如图是A、B两种物质的溶解度曲线,请回答: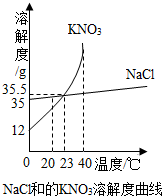 用科学方法认识和改造物质
用科学方法认识和改造物质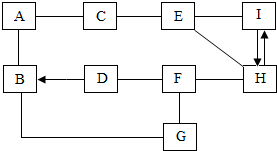 已知A-I均为初中化学常见的物质,它们相互间的关系如图所示.该图体现了化合物F四种不同的化学性质,其中B溶液呈蓝色,I是无色无味的气体,B、C分别与A反应均有不溶于稀硝酸的同种白色沉淀产生,E与F反应生成另一种不溶于稀硝酸的白色沉淀,C与E反应产生氨味气体.(“-”表示两物质间能反应,“→”表示物质间的转化关系.)
已知A-I均为初中化学常见的物质,它们相互间的关系如图所示.该图体现了化合物F四种不同的化学性质,其中B溶液呈蓝色,I是无色无味的气体,B、C分别与A反应均有不溶于稀硝酸的同种白色沉淀产生,E与F反应生成另一种不溶于稀硝酸的白色沉淀,C与E反应产生氨味气体.(“-”表示两物质间能反应,“→”表示物质间的转化关系.)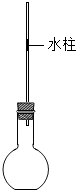 有关NaOH与CO2反应的探究
有关NaOH与CO2反应的探究