题目内容
9.某氯化钾样品含有杂质氯化钙和氯化镁,实验室提纯流程如下: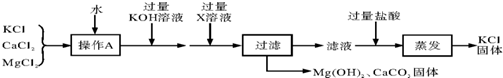
(1)操作A的目的是使溶解形成溶液,X溶液中溶质是K2CO3.
(2)过滤时用到的玻璃仪器有漏斗、烧杯、玻璃棒.实验过程中发现过滤速度较慢,可能的原因是固体颗粒阻碍了液体通过滤纸孔隙,还可能是滤纸下面有气泡.本实验中蒸发是为了除去H2O、HCl(填化学式).
(3)若样品中含80g KCl,理论上最终所得 KCl固体的质量A(填编号).
A.大于 80g B.等于 80g C.小于 80g D.无法确定.
分析 (1)根据加入水的目的是使样品充分溶解;根据流程图分析,加入氢氧化钾可以除去氯化镁,除去氯化钙而又不增加新的杂质用碳酸钾溶液进行分析;
(2)根据根据过滤所用仪器及注意事项分析解答;
根据盐酸具有挥发性及蒸发原理分析所除的物质;
(3)根据反应后溶液的成分进行分析.
解答 解:(1)加入水的目的是使样品充分溶解形成溶液,便于实验;根据流程图分析,加入氢氧化钾可以除去氯化镁,除去氯化钙而又不增加新的杂质用碳酸钾溶液;
(2)过滤所用的玻璃仪器是烧杯、漏斗和玻璃棒;实验过程中发现过滤速度较慢,可能的原因是固体颗粒阻碍了液体通过滤纸孔隙,还可能是滤纸没紧贴漏斗内壁,中间留有气泡或滤纸的规格不对等;蒸发可以除去溶液中的水分,而盐酸具有挥发性,可以挥发出氯化氢气体,所以同时还可以除去溶液中的氯化氢;
(3)最后的氯化钾固体中包括了过量的碳酸钾、氢氧化钾和盐酸反应生成的氯化钾,还有氢氧化钾和氯化镁反应生成的氯化钾,所以最终所得氯化钾固体大于80g,故选:A.
故答案为:(1)溶解形成溶液,K2CO3;
(2)玻璃棒,滤纸下面有气泡,H2O、HCl;
(3)A.
点评 本题主要考查了物质的提纯实验的相关的操作要领以及物质除杂的原则,要明确流程图中每一步的作用,再结合题意细致分析解答.

练习册系列答案
相关题目
4.小Q同学为了比较X、Y、Z、W四种 金属的活动性顺序,进行有关实验,结果如表(“√”表示能反应,“-”表示不能反应,“空白”表示未做该实验).请你判断四种金属的活动性顺序为( )
| X | Y | Z | W | |
| 稀盐酸 | √ | - | - | √ |
| Y的硝酸盐溶液 | √ | √ | ||
| W的硝酸盐溶液 | √ | - |
| A. | Z>Y>X>W | B. | X>Z>W>Y | C. | X>W>Z>Y | D. | W>X>Z>Y |
14.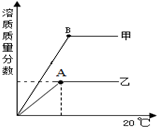 20℃时,等量水中,分别加入甲、乙两种固体,溶质质量分数变化如图,说法错误的是( )
20℃时,等量水中,分别加入甲、乙两种固体,溶质质量分数变化如图,说法错误的是( )
 20℃时,等量水中,分别加入甲、乙两种固体,溶质质量分数变化如图,说法错误的是( )
20℃时,等量水中,分别加入甲、乙两种固体,溶质质量分数变化如图,说法错误的是( )| A. | A点所示乙溶液中,加入少量固体甲,能继续溶解 | |
| B. | 20℃时,甲的溶解度大于乙的溶解度 | |
| C. | 将A、B点两种物质的溶液,降温,均有晶体析出 | |
| D. | 由图可知,影响固体物质溶解度的因素:溶质种类 |
19.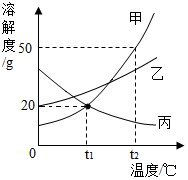 如图是甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.下列说法正确的是( )
 如图是甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.下列说法正确的是( )| A. | t1℃时,甲、丙的饱和溶液中溶质与溶液的质量比均为1:5 | |
| B. | t2℃时,物质甲的饱和溶液的溶质质量分数为50% | |
| C. | 将甲、乙的饱和溶液分别从t1℃升温到t2℃,不考虑水的蒸发溶质质量分数都不变 | |
| D. | 升高丙溶液的温度,一定有晶体析出 |
 向53g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为5%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如图所示.(不考虑CO2的溶解)
向53g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为5%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如图所示.(不考虑CO2的溶解)