题目内容
17.某些金属氢化物(其中氢显-1价)与水反应可生成碱和氢气,如NaH+H2O═NaOH+H2↑,CaH2与H2O的反应和NaH相似.试用化学方程式表示CaH2与H2O发生的化学反应:CaH2+2H2O=Ca(OH)2+2H2↑.分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:氢化钠(NaH)与水反应的化学方程式为NaH+H2O=NaOH+H2↑,CaH2与NaH的化学性质相似,则CaH2与水反应生成氢氧化钙和氢气,反应的化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑.
故答案为:CaH2+2H2O=Ca(OH)2+2H2↑
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.化学研究物质的性质和用途,请体会并填写下表:
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 | 氧气用于炼钢 | 干冰用于人工降雨 | 氮气保护食品 |
| 对应特性 | ①硬度最大 | ②良好的导电性 | ③吸附性 | ④氧化性 | ⑤易升华 | ⑥性质稳定 |
9. 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe,Fe2O3,CaO,Ca(OH)2和CaCO3.
【实验探究】
甲同学的方案:
乙同学认为甲同学的实验并不能得出一定不含Fe203的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.并设计如下实验方案继续验证.

(1)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(2)乙同学对滤渣B又进行探究.
【反思与评价】
丙同学认为乙同学的方案中仍有一种物质不能确定.丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaC03的质量为1.Og,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe,Fe2O3,CaO,Ca(OH)2和CaCO3.
【实验探究】
甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管 中,滴加足量的稀盐酸 | 固体逐渐消失,有大 量无色气体产生,得 到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe203. |

(1)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(2)乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 固体中一定含有CaC03和Fe203. |
丙同学认为乙同学的方案中仍有一种物质不能确定.丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaC03的质量为1.Og,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
6. 下表列出了硝酸钾在不同温度下的溶解度.
下表列出了硝酸钾在不同温度下的溶解度.
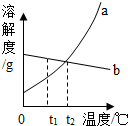
(1)从上表你可以得到什么信息(写一条即可)?硝酸钾的溶解度随温度的升高而增大(写一条即可).硝酸钾的溶解度曲线与图中曲线a(选填“a”或“b”)相吻合.
(2)60℃时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:10;欲使该温度时一定量的硝酸钾不饱和溶液变为饱和溶液,可采取的措施是增加溶质.
(3)将t2℃a、b两种物质的饱和溶液降温至t1℃,溶液中溶质质量分数不变的是b.
 下表列出了硝酸钾在不同温度下的溶解度.
下表列出了硝酸钾在不同温度下的溶解度. | 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度(g) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(2)60℃时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:10;欲使该温度时一定量的硝酸钾不饱和溶液变为饱和溶液,可采取的措施是增加溶质.
(3)将t2℃a、b两种物质的饱和溶液降温至t1℃,溶液中溶质质量分数不变的是b.
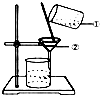 如图所示.(1)该图进行的是过滤操作.在此操作中玻璃棒的作用是引流,滤纸的边缘要高于液面(填“高于”或“低于”).
如图所示.(1)该图进行的是过滤操作.在此操作中玻璃棒的作用是引流,滤纸的边缘要高于液面(填“高于”或“低于”).