题目内容
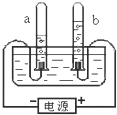 电解水实验:
电解水实验:(1)负极产生的是
(2)电解水的实验说明
(3)保持水的化学性质微粒的是
(4)化学方程式为
(5)若实验观察到的现象是A、B两极气体的体积比小于理论值,可能的原因是
考点:电解水实验,分子的定义与分子的特性,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:根据电解水的实验的现象和结论分析回答.在电解水时,正极产生的气体是氧气,能支持燃烧;负极产生的气体是氢气,能燃烧.二者的体积比是1:2,该实验证明了水是由氢元素和氧元素组成,根据反应写出反应的化学方程式.
解答:解:(1)由电解水的装置可知,与电源负极相连的a试管内收集的气体较多是氢气,液面下降较快.与电源正极相连的b试管内收集的气体较少是氧气,试管a与试管b内气体的体积比为:2:1,质量比为1:8;故填:氢气;氧气;2:1;1:8;
(2)电解水生成了氢气和氧气.证明了水是由氢和氧两种元素组成的;故填:水是由氢和氧两种元素组成的;
(3)在化学变化中分子可以再分,而原子不能再分,所以保持水的化学性质微粒的是水分子;在电解水的过程中发生改变的微粒是水分子;不变的微粒是氢原子和氧原子;生成新的微粒是氢分子和氧分子;故填:水分子;水分子;氢原子和氧原子;氢分子和氧分子;
(4)水在通电的条件下生成了氢气和氧气,发生反应的化学方程式为:2H2O
2H2↑+O2↑;故填:2H2O
2H2↑+O2↑;
(5)若实验观察到的现象是A、B两极气体的体积比小于理论值,可能的原因是氧气比氢气更容易溶于水、装置漏气等.故填:氧气比氢气更容易溶于水.
(2)电解水生成了氢气和氧气.证明了水是由氢和氧两种元素组成的;故填:水是由氢和氧两种元素组成的;
(3)在化学变化中分子可以再分,而原子不能再分,所以保持水的化学性质微粒的是水分子;在电解水的过程中发生改变的微粒是水分子;不变的微粒是氢原子和氧原子;生成新的微粒是氢分子和氧分子;故填:水分子;水分子;氢原子和氧原子;氢分子和氧分子;
(4)水在通电的条件下生成了氢气和氧气,发生反应的化学方程式为:2H2O
| ||
| ||
(5)若实验观察到的现象是A、B两极气体的体积比小于理论值,可能的原因是氧气比氢气更容易溶于水、装置漏气等.故填:氧气比氢气更容易溶于水.
点评:本题主要考查了学生对于电解水实验的理解和掌握,要求同学平时学习的过程中积极的参与实验,并分析实验得出正确的结论.

练习册系列答案
相关题目
以下面两组物质都按相同的规律排列:
①BaSO4、H2O、HCl、Ca(OH)2 ②NaCl、P2O5、 、NaOH
请找出排列规律,判断在②的横线处的物质是( )
①BaSO4、H2O、HCl、Ca(OH)2 ②NaCl、P2O5、 、NaOH
请找出排列规律,判断在②的横线处的物质是( )
| A、CaO |
| B、CuSO4 |
| C、H2SO4 |
| D、Mg(OH)2 |
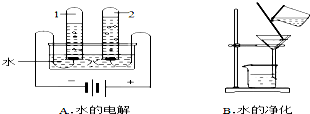
 实验室按图制取CO2并检验CO2的性质,试回答下列问题
实验室按图制取CO2并检验CO2的性质,试回答下列问题