题目内容
13.下列说法正确的是( )| A. | O和O2-都是氧元素,所以它们的化学性质相同 | |
| B. | 化学式为AB型的离子化合物中,阴阳离子所带电荷的数值必然相等 | |
| C. | m g食盐和n g水充分振荡,形成的溶液的质量一定是(m+n)g | |
| D. | 纯净物一定是由同种元素组成的物质 |
分析 A、原子或离子(简单离子)的化学性质与其最外层电子数有关;
B、根据物质呈电中性分析判断;
C、食盐不一定完全溶于水中;
D、纯净物只含同一种物质.
解答 解:A、氧原子和氧离子最外层电子数不同,所以其化学性质不同,故A错误;
B、物质呈电中性,物质中阴阳离子所带电量相等,化学式为AB型的离子化合物中,阴阳离子个数之比是1:1,所以阴阳离子所带电荷的数值必然相等,故B正确;
C、如果形成的是过饱和溶液,部分食盐不溶于水,会导致溶液的质量小于(m+n)g,故C错误;
D、纯净物只含同一种物质,由同种元素组成的物质可能是单质也可能是混合物,故D错误;
故选B.
点评 本题考查了纯净物的判断、微粒的化学性质等知识点,易错选项是C,常常认为所给食盐都溶于水导致作出错误判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列图示的实验操作正确的是( )
| A. | 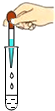 | B. |  | C. | 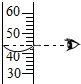 | D. | 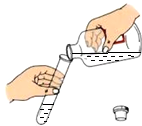 |
4.如图所示实验操作不正确的是( )
| A. | 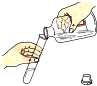 倾倒液体 | B. | 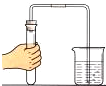 检查气密性 | C. | 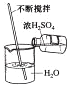 稀释浓硫酸 | D. | 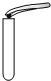 取用固体 |
1.1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g,水两种物质,关于该物质的组成有以下论断
①一定含碳、氢两种元素
②一定含有氧元素
③可能含有氧元素
④一定不含有氧元素
⑤该物质分子中碳、氢的原子个数比为1:2
⑥物质分子中碳、氢的原子个数比为 1:4,
其中叙述正确的是( )
①一定含碳、氢两种元素
②一定含有氧元素
③可能含有氧元素
④一定不含有氧元素
⑤该物质分子中碳、氢的原子个数比为1:2
⑥物质分子中碳、氢的原子个数比为 1:4,
其中叙述正确的是( )
| A. | ①②⑤ | B. | ①④⑤ | C. | ①④⑥ | D. | ①③⑥ |
8.下列归纳和总结完全正确的一组是( )
| A.性质与用途 ①O2助燃--气焊切割金属 ②电解水产生O2--实验室制O2 | B.分离或鉴别方法与原理 ①用燃着的木条鉴别氢气、氧气、二氧化碳--化学性质不同 ②石油分离出汽油、煤油、柴油等--物质沸点不同 |
| C.日常生活经验 ①区别硬水与软水--常用肥皂水 ②防止煤气中毒--在室内放一盆水 | D.化学概念的逻辑关系 ①分解反应与化合反应--并列关系 ②化合物与氧化物--交叉关系 |
| A. | A | B. | B | C. | C | D. | D |
5.根据下列金属的熔沸点:
其中不能形成合金的是( )
| 金属 | Na | Cu | Al | Fe |
| 熔点(℃) | 97.5 | 1 083 | 660 | 1 535 |
| 沸点(℃) | 883 | 2 595 | 2 200 | 3 000 |
| A. | Cu与Al | B. | Fe与Cu | C. | Fe与Na | D. | Al与Na |
3.科学探究中常用到推理的方法.根据如表实验事实推出结论正确的是( )
| 编号 | 实验事实 | 实验结论 |
| A | 某溶液使酚酞溶液变红 | 该溶液一定是NaOH溶液 |
| B | 某物质中含有一种元素 | 该物质一定是单质 |
| C | 常温下,测定某溶液的PH=3 | 该溶液一定呈酸性 |
| D | 某气体不能使带火星的木条复燃 | 该气体一定不含氧气 |
| A. | A | B. | B | C. | C | D. | D |