题目内容
4.某化学兴趣小组通过实验对碱的化学性质进行验证和总结,如图所示,请回答下列问题:
(1)甲同学将酚酞溶液滴入Ca(OH)2溶液中,观察到溶液变红,得出结论:Ca(OH)2溶液呈碱性(填“酸性”、“碱性”或“中性”).
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质有氯化钙和氯化氢(酸碱指示剂除外).
(3)丙同学根据反应③得出结论:实验室存放碱溶液时需密封保存.
(4)丁同学选用氢氧化钠溶液与氯化钾溶液来验证性质④,但发现两种不反应,由此得出结论:碱能与某些盐发生化学反应.
分析 (1)氢氧化钙溶液显碱性,能使酚酞试液变红色;
(2)氢氧化钙能和稀盐酸反应生成氯化钙和水,显酸性或显中性的溶液不能使酚酞试液变色;
(3)反应③中,由于碱能和某些非金属氧化物反应,因为空气中含有二氧化碳,因此实验室存放碱溶液时需密封;
(4)氢氧化钠与氯化钾不能反应,说明碱不能和所有盐反应,而是能和某些盐反应.
解答 解:(1)甲同学将酚酞溶液滴入Ca(OH)2溶液中,观察到溶液变红,得出结论:Ca(OH)2溶液呈碱性.
故填:碱性.
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到红色褪去,说明氢氧化钙已经完全反应,此时所得溶液中含有的溶质有反应生成的氯化钙和过量的氯化氢.
故填:氯化钙和氯化氢.
(3)反应③中,由于碱能和某些非金属氧化物反应,因为空气中含有二氧化碳,因此实验室存放碱溶液时需密封.
故填:密封保存.
(4)丁同学选用氢氧化钠溶液与氯化钾溶液来验证性质④,但发现两种不反应,由此得出结论:碱不能和所有盐反应,而是能和某些盐反应.
故填:碱能与某些盐发生化学反应.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
18.茶叶包装已经是中国茶叶产业重要环节,下列包装材料属于合金的是( )
| A. | 陶瓷茶叶罐 | B. | 玻璃茶叶罐 | C. | 马口铁茶叶罐 | D. | 纸制茶叶罐 |
19.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是( )
| A. | 分离CO2和CO,先用NaOH溶液吸收CO2,再向该溶液中加足量稀盐酸 | |
| B. | 只用一种试剂无法把稀盐酸、氯化钡溶液和硝酸钾三种溶液区别开 | |
| C. | 除去氯化钙溶液中混有的少量稀盐酸,可加入过量碳酸钙,充分反应后过滤 | |
| D. | 只用组内溶液相互混合方法,能将KOH、Na2SO4、CuSO4、MgCl2鉴别开 |
16.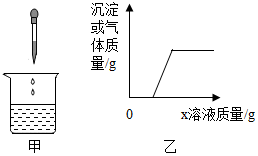 向烧杯中逐滴加入X溶液至过量(图甲所示),生成沉淀或气体的质量与加入X溶液的质量关系符合图乙所示的是( )
向烧杯中逐滴加入X溶液至过量(图甲所示),生成沉淀或气体的质量与加入X溶液的质量关系符合图乙所示的是( )
 向烧杯中逐滴加入X溶液至过量(图甲所示),生成沉淀或气体的质量与加入X溶液的质量关系符合图乙所示的是( )
向烧杯中逐滴加入X溶液至过量(图甲所示),生成沉淀或气体的质量与加入X溶液的质量关系符合图乙所示的是( )| 烧杯中的物质 | X溶液 | |
| A | HCl和FeCl3溶液 | NaOH溶液 |
| B | 碳酸氢钠和氯化钠溶液 | 稀HCl |
| C | 镁铝合金 | 稀HCl |
| D | 稀盐酸和稀硫酸 | BaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |