题目内容
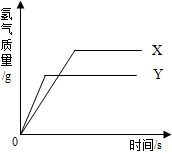 现有等质量的X、Y两种金属(化合价都为+2价),分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如下图所示.下列说法中正确的是( )
现有等质量的X、Y两种金属(化合价都为+2价),分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如下图所示.下列说法中正确的是( )| A、生成氢气的质量:X<Y |
| B、相对原子质量:X>Y |
| C、金属活动性:X>Y |
| D、消耗硫酸的质量:X>Y |
考点:金属的化学性质
专题:金属与金属材料
分析:A、根据图象分析生成氢气的质量;
B、根据等质量的金属与足量的稀硫酸完全反应,产生氢气的质量与金属的相对原子质量成反比分析;
C、据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断三种金属活动性;
D、根据质量守恒定律定律可知,生成氢气的质量取决于消耗的硫酸的质量.
B、根据等质量的金属与足量的稀硫酸完全反应,产生氢气的质量与金属的相对原子质量成反比分析;
C、据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断三种金属活动性;
D、根据质量守恒定律定律可知,生成氢气的质量取决于消耗的硫酸的质量.
解答:解:A、根据反应生成H2的质量与反应时间的关系图所示,在两种金属完全反应后,放出H2的质量是X>Y,正确;
B、X、Y金属的质量都相等(化合价都为+2价),完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在金属完全反应后,放出H2的质量是X>Y,因此可判断相对原子质量是Y>X,故说法错误;
C、根据反应生成H2的质量与反应时间的关系图所示,相同时间内Y放出氢气的质量大于X,可判断金属活动性顺序是Y>X,故说法正确;
D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:X>Y,故说法正确;
故选B.
B、X、Y金属的质量都相等(化合价都为+2价),完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在金属完全反应后,放出H2的质量是X>Y,因此可判断相对原子质量是Y>X,故说法错误;
C、根据反应生成H2的质量与反应时间的关系图所示,相同时间内Y放出氢气的质量大于X,可判断金属活动性顺序是Y>X,故说法正确;
D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:X>Y,故说法正确;
故选B.
点评:活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比,据此结合图象细心分析解答.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案
相关题目
现在社会提倡“节能、环保、低碳”.下列活动不符合上述理念的是( )
| A、停止含碳矿物的开采和加工 |
| B、积极开发使用风能、太阳能等新能源,减少化石燃料的使用 |
| C、尽量减少含碳物质的排放和浪费 |
| D、在生产和生活中提倡使用节能技术和节能产品 |
通过一年的化学学习,请你判断下列过程中不包含化学变化的是( )
| A、干旱时期用干冰进行人工降雨 |
| B、用天然气做燃料做饭 |
| C、绿色植物进行光合作用 |
| D、家庭用醋酸除去水壶内的水垢 |
X溶液与AgNO3、Na2CO3、Na2SO4三种溶液反应均有白色沉淀产生,则X可能是( )
| A、HCl |
| B、H2SO4 |
| C、Ca(OH)2 |
| D、BaCl2 |
下列应用的原理(用符号表达式表示)及基本反应类型均正确的是( )
| A、碳酸钙与盐酸反应CaCO3+HCl→CaCl2+H2O+CO2↑ 分解反应 | |||
B、拉瓦锡测定空气中氧气含量实验Hg+O2
| |||
C、加热混有二氧化锰的氯酸钾制取氧气KClO3
| |||
D、氢气在氯气中燃烧H2+Cl2
|
某化学反应中,各物质质量随时间变化的曲线如图所示.其中说法一定正确的是( )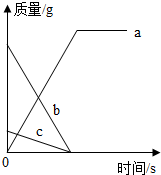

| A、该反应是分解反应 |
| B、物质c发生还原反应 |
| C、物质a的摩尔质量等于b和c的摩尔质量之和 |
| D、物质a中元素种类等于b和c中元素种类之和 |