题目内容
16.胃酸(gastric acid)指胃液中分泌的盐酸.胃酸在食物的消化过程中起着极其重要的作用.如①杀死随食物及水进入胃内的细菌.②分解食物中的结缔组织和肌纤维,使食物中的蛋白质变性,易于被消化.③与钙和铁结合,形成可溶性盐,促进它们的吸收.胃酸的量不能过多,当胃酸过多时医生通常是用“小苏打片”“胃舒平”等药物进行治疗.小苏打的成分主要是碳酸氢钠,胃舒平中则主要含有氢氧化铝.请写出小苏打与盐酸反应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑,经研究发现,长期使用我国发明的铁锅炒菜做饭,可减少缺铁性贫血的发生,原因是少量单质铁会随着饭菜进入胃中,与胃酸反应,生成易被人体吸收的铁元素,请写出铁与盐酸反应的化学方程式Fe+2HCl=FeCl2+H2↑.分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.小苏打的主要成分是碳酸氢钠,和盐酸反应生成氯化钠、水和二氧化碳.金属和酸反应生成氢气,必须具备以下条件:金属必须是在金属活动性顺序中氢前的金属,酸除浓硫酸和硝酸外.
解答 解:小苏打的主要成分是碳酸氢钠,它与胃酸中盐酸反应的化学方程式是:NaHCO3+HCl═NaCl+H2O+CO2↑.
由于铁在金属活动性顺序中位于氢前,胃酸中含有盐酸,随饭菜进入到胃中的铁就和胃酸中的盐酸反应生成人体易吸收的亚铁离子;
反应物是铁与盐酸,生成物是氯化亚铁和氢气,用观察法配平,氢气后面标上上升符号,所以方程式是:Fe+2HCl=FeCl2+H2↑;
故答案为:NaHCO3+HCl═NaCl+H2O+CO2↑;少量单质铁会随着饭菜进入胃中,与胃酸反应,生成易被人体吸收的铁元素;Fe+2HCl=FeCl2+H2↑;
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
6.有关铁的试验现象的描述,正确的是( )
| A. | 将连着一根点燃火柴的细铁丝伸入氧气瓶中,铁丝剧烈燃烧,火焰四射 | |
| B. | 将一枚铁钉的一端浸入水中,另一端露在空气中,数日后看到铁钉表面有一层红色疏松的铁锈 | |
| C. | 将铁粉放入稀盐酸中,冒出气泡,溶液由无色逐渐变成黄色 | |
| D. | 将铁钉放入CuSO4晶体中,铁钉表满覆盖了一层铜 |
7.通过观察蜡烛的燃烧以及对燃烧产物的实验探究,正确的结论是( )
①火焰温度最高处是外焰
②蜡烛燃烧能生成二氧化碳和水
③燃烧时可产生发光发热的现象
④熄灭后产生的白烟是石蜡小颗粒.
①火焰温度最高处是外焰
②蜡烛燃烧能生成二氧化碳和水
③燃烧时可产生发光发热的现象
④熄灭后产生的白烟是石蜡小颗粒.
| A. | 只有①②③ | B. | 只有②③④ | C. | 只有④ | D. | ①②③④ |
4.下列四种粒子的结构示意图中,说法正确的是( )
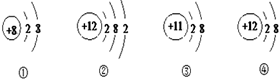

| A. | 它们表示四种不同的元素 | |
| B. | ①③④表示的微粒具有相同的核外电子排布 | |
| C. | ①③④表示的元素都是非金属元素,其化学性质相似 | |
| D. | ①④表示的是阳离子 |
11.下列各组数据中,符合质量守恒定律的是( )
| A. | 32g硫和16g氧气反应,生成48g二氧化硫 | |
| B. | 2g氢气和16g氧气反应,生成18g水 | |
| C. | 3g碳和10g氧气充分反应,生成13g二氧化碳 | |
| D. | 3g镁和3 g氧气充分反应生成6g氧化镁 |
1.制造下列物质时,不需要用石灰石作原料的是( )
| A. | 生铁 | B. | 生石灰 | C. | 水泥 | D. | 钢 |
8.下列过程不属于缓慢氧化的是( )
| A. | 动物呼吸 | B. | 钢铁生锈 | C. | 橡胶老化 | D. | 纸张燃烧 |
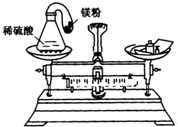 物质发生化学变化的前后,总质量是否发生了改变?请你和小明按下面的过程一起探究:
物质发生化学变化的前后,总质量是否发生了改变?请你和小明按下面的过程一起探究: