题目内容
20.洁净的空气对于人类和其他动植物都是非常重要的,但随着工业发展,空气遭到污染,空气污染的来源有哪些工厂排放的废气,如何保护空气植树造林(各写一条即可).
分析 空气污染来源于煤、石油等燃料的燃烧,工厂排放的废气等;要减少含硫煤的使用、多植树造林、使用自行车、新能源汽车、少放烟花爆竹等.
解答 解:空气污染来源于煤、石油等燃料的燃烧,工厂排放的废气等;空气污染会造成酸雨腐蚀建筑物,危害人体健康等,二氧化硫是造成酸雨的罪魁祸首,因此要减少含硫煤的使用、多植树造林、使用自行车、新能源汽车、少放烟花爆竹等;提倡节能环保,低碳经济.
故答案为:工厂排放的废气;植树造林.
点评 本考点主要是空气的污染及其危害,空气污染的途径主要有两个:有害气体和粉尘.环保问题已经引起了全球的重视,关于“三废”的处理问题,是中考的热点问题,同学们要认真掌握.

练习册系列答案
相关题目
8.下列操作或现象与分子对应的特性不一致的选项是( )
| 选项 | 操作、现象或事实 | 分子的特性 |
| A | 气体容易被压缩 | 分子间有间隙 |
| B | 一滴水中含有1.67×1021个水分子 | 分子很小 |
| C | 物体热胀冷缩 | 分子可变大或变小 |
| D | 墙内开花墙外香 | 分子在不停地运动 |
| A. | A | B. | B | C. | C | D. | D |
15.根据如图回答问题.
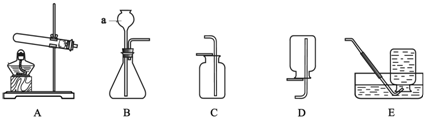
(1)实验仪器a的名称是长颈漏斗.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,所选用的发生装置是A(填字母序号).
(3)用大理石和稀盐酸制取二氧化碳应选用的发生装置为B,收集二氧化碳所选用的装置为C(填字母序号).
(4)实验反思:在加热KClO3制O2的过程中,发现产生O2的速率很慢,经检查不是KClO3变质,也不是装置气密性不好,你认为最可能的原因是没有使用催化剂.若收集到的氧气不纯,可能的原因为装置漏气(答一条即可)
(5)为了检测某石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试回答:
①样品中碳酸钙的质量分数为80%.
②12.5g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)

(1)实验仪器a的名称是长颈漏斗.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,所选用的发生装置是A(填字母序号).
(3)用大理石和稀盐酸制取二氧化碳应选用的发生装置为B,收集二氧化碳所选用的装置为C(填字母序号).
(4)实验反思:在加热KClO3制O2的过程中,发现产生O2的速率很慢,经检查不是KClO3变质,也不是装置气密性不好,你认为最可能的原因是没有使用催化剂.若收集到的氧气不纯,可能的原因为装置漏气(答一条即可)
(5)为了检测某石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 12.5 | 12.5 | 12.5 | 12.5 |
| 加入盐酸的质量(g) | 40.0 | 50.0 | 65.0 | 80.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 2.5 | 2.5 |
①样品中碳酸钙的质量分数为80%.
②12.5g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)
9.下列变化属于化学变化的是( )
| A. | 工业制氧气 | B. | 活性炭吸附水中的色素 | ||
| C. | 煤矿瓦斯爆炸 | D. | 蒸发食盐水 |
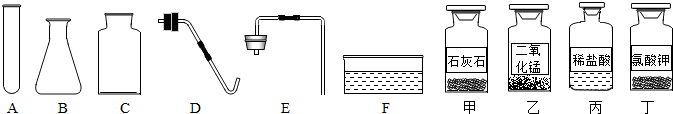
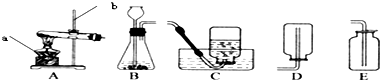
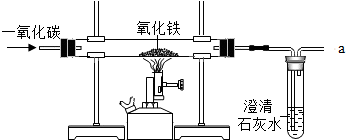
 黄铜(铜锌合金)是重要的金属材料.为测定黄铜材料中锌的含量,化学研究小组进行了实验:
黄铜(铜锌合金)是重要的金属材料.为测定黄铜材料中锌的含量,化学研究小组进行了实验: