题目内容
19.为了更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念.若从酸度(AG)的概念出发可得出结论:酸性溶液的AG>0,中性溶液的AG=0,碱性溶液的AG<0.下列说法中不正确的是( )| A. | AG的值越大,溶液的pH越小 | B. | 若某溶液的AG=0,则该溶液的pH=0 | ||
| C. | 25℃时,纯水的AG=0,pH=7 | D. | 25℃时,pH>7的溶液中AG<0 |
分析 盐溶液中,有的显酸性,有的显中性,有的显碱性;
AG的值越大,溶液的酸性越强;
25℃时,纯水显中性,PH等于7;
25℃时,PH>7的溶液显碱性.
解答 解:A、AG的值越大,溶液的酸性越强,溶液的PH越小.正确;
B、若某溶液的AG=0,为中性溶液,则该溶液的pH=0.正确;
C、25℃时,纯水中的AG=0,PH=7.正确;
D、25℃时,PH>7的溶液显碱性,则AG<0.正确.
故选B.
点评 解答本题要充分理解溶液的酸度和溶液的酸碱度之间的关系,解答时要从酸度与酸碱度的关系方面进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14 | |
| B. | 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等 | |
| C. | 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量不相等 | |
| D. | 等质量的质量分数均为4%氢氧化钠溶液与稀盐酸充分反应,所得溶液显中性 |
4.不用试剂,鉴别下列5种物质的溶液:①Ba(OH)2;②FeCl3;③BaCl2;④H2SO4;⑤KCl被鉴别出物质的先后顺序是( )
| A. | ④③①②⑤ | B. | ②①④③⑤ | C. | ②④①③⑤ | D. | ④①②③⑤ |
11.向盛有酚酞和NaOH溶液的烧杯中滴加稀盐酸,直至液体呈无色.为探究反应后溶液中溶质的组成,所选试剂不正确的是( )
| A. | 氢氧化钠溶液 | B. | 锌粒 | C. | 碳酸钠溶液 | D. | 紫色石蕊溶液 |
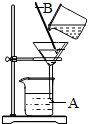 如图是实验室中过滤操作示意图,回答下列问题:
如图是实验室中过滤操作示意图,回答下列问题: 某科学小组为了测定石膏的组成(CaS04.xH20),即测x值,做了如下实验:将含结晶水的硫酸钙放在钳锅中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长.他们在实验中将数据整理如表.利用数据可绘制成如图的图象:
某科学小组为了测定石膏的组成(CaS04.xH20),即测x值,做了如下实验:将含结晶水的硫酸钙放在钳锅中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长.他们在实验中将数据整理如表.利用数据可绘制成如图的图象: