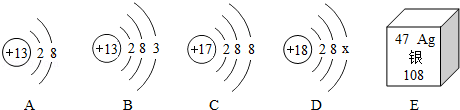
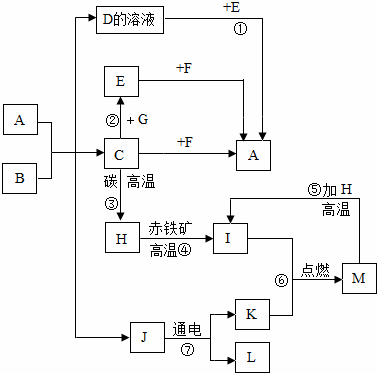
题目内容
已知某粗盐样品中含有Na2SO4、MgCl2、CaCl2等杂质.实验室提纯流程如下:
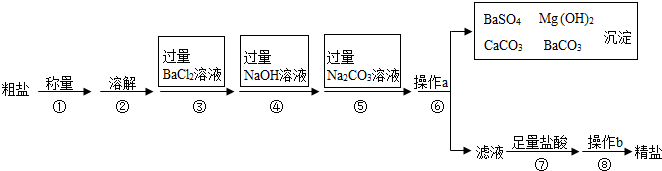
(1)用托盘天平称量粗盐时,若指针偏向右边,则表示(填下列正确选项的代码) .
A.右盘重,砝码轻 B.右盘轻,样品重
C.左盘重,样品轻 D.左盘轻,砝码重
(2)第④步操作发生反应的化学方程式是 .
(3)第⑤步操作的目的是 .
(4)第⑥步操作a的名称是 ,此步操作中,玻璃棒的末端要轻轻地斜靠在 的一边.
(5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是 .
(6)在第⑧步操作时,要用玻璃棒不断搅拌,目的是 .
| 氯化钠与粗盐提纯;称量器-托盘天平;盐的化学性质;书写化学方程式、文字表达式、电离方程式.版权所有 | |
| 专题: | 压轴实验题;常见的盐 化学肥料. |
| 分析: | (1)根据称量物质是“左物右码”进行解答; (2)根据加入过量氢氧化钠溶液的目的是除去氯化镁进行解答; (3)根据加入过量的碳酸钠溶液的目的除去杂质CaCl2和加入的过量试剂BaCl2进行解答; (4)根据过滤用于分离难溶性固体和可溶性固体的方法进行解答; (5)根据在第⑦步操作中,向滤液中滴加足量盐酸的目的是除去加入的过量试剂NaOH和Na2CO3进行解答; (6)根据蒸发结晶过程中玻璃棒的作用进行解答. |
| 解答: | 解:(1)称量物质是“左物右码”,所以用托盘天平称量粗盐时,若指针偏向右边,则表示左盘轻,砝码重; (2)加入过量氢氧化钠溶液的目的是除去氯化镁,发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl; (3)加入过量的碳酸钠溶液的目的除去杂质CaCl2和加入的过量试剂BaCl2; (4)过滤用于分离难溶性固体和可溶性固体的方法,第⑥步操作a的名称是过滤,此步操作中,玻璃棒的末端要轻轻地斜靠在三层滤纸的一边; (5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是除去加入的过量试剂NaOH和Na2CO3; (6)蒸发结晶过程中玻璃棒的作用:防止蒸发时因局部温度过高,造成液滴飞溅. 故答案为:(1)D; (2)MgCl2+2NaOH=Mg(OH)2↓+2NaCl; (3)除去杂质CaCl2和加入的过量试剂BaCl2; (4)过滤;三层滤纸; (5)除去加入的过量试剂NaOH和Na2CO3; (6)防止蒸发时因局部温度过高,造成液滴飞溅. |
| 点评: | 本题从多个角度对氯化钠的提纯实验进行了全面考察,灵活性强. |

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案以下四组离子,有一组能大量共存且能形成无色透明溶液,它应该是( )
|
| A. | Fe3+ SO42﹣ H+ Cl﹣ | B. | Mg2+ Cl﹣ OH﹣ Na+ |
|
| C. | H+ Ba2+ NO3﹣ SO42﹣ | D. | H+ Na+ K+ NO3+ |
| 加稀盐酸质量(g) | 剩余固体质量(g) | |
| 1 | 10 | 5.5 |
| 2 | 10 | m |
| 3 | 10 | 1.2 |
| 4 | 10 | 1.2 |
同学前往当地矿区进行调查,他取回若干小块矿石样品,对其中的CaCO3的质量分数进行检测,采用以下方法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据如下(样品中杂质不溶于水,不与酸反应) 计算:
(1)样品中的CaCO3的质量分数 ;
(2)表中m的数值应为 ;
(3)所用稀盐酸的溶质质量分数?
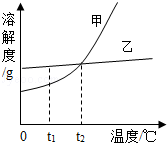
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
|
| A. | 甲物质的溶解度一定大于乙物质的溶解度 |
|
| B. | t2℃时,甲、乙饱和溶液的溶质质量分数相等 |
|
| C. | 将甲溶液从t2℃时降温到t1℃时,一定有晶体析出 |
|
| D. | 将t2℃时乙的饱和溶液变为不饱和溶液,可采取降温的方法 |