题目内容
19.下列何组物质是按酸、碱、盐顺序排列的( )| A. | H2CO3、NaCl、Mg(OH)2 | B. | Ca(OH)2、HCl、Na2SO4 | ||
| C. | MgSO4、H2SO4、HCl | D. | CH3COOH、NaOH、Na2CO3 |
分析 根据酸、碱、盐的组成特点进行分析.电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子和酸根离子组成的化合物是盐.
解答 解:A、碳酸电离时生成的阳离子都是氢离子,属于酸;氯化钠是由钠离子和氯离子组成的化合物,属于盐;氢氧化镁是由镁离子和氢氧根离子组成的化合物,属于碱.故选项错误;
B、氢氧化钙电离时生成的阴离子都是氢氧根离子,属于碱;盐酸电离时生成的阳离子都是氢离子,属于酸;硫酸钠是由钠离子和硫酸根离子组成的化合物,属于盐.故选项错误;
C、硫酸镁电离时生成的镁离子和硫酸根离子,属于盐;硫酸电离时生成的阳离子都是氢离子,属于酸;盐酸电离时生成的阳离子都是氢离子,属于酸.故选项错误;
D、醋酸电离时生成的阳离子都是氢离子,属于酸;氢氧化钠电离时生成的阴离子都是氢氧根离子,属于碱;碳酸钠是由钠离子和碳酸根离子组成的化合物,属于盐.故选项正确.
故选D.
点评 本题主要考查物质的分类,解答时要分析物质的元素组成和阴阳离子组成,然后再根据酸碱盐概念方面进行分析、判断,从而得出正确的结论.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
10.下列有关金属材料的说法中不正确的是( )
| A. | 纯金属和合金都属于金属材料 | |
| B. | 金属铜通常用作导线是因为它的导电性最好 | |
| C. | 常温下不是所有金属都是固体 | |
| D. | 金属一定是单质,合金一定是混合物 |
4.在稀硫酸中含有H2O分子、H+离子和SO42-离子,为了证明究竟是这三种粒子中的哪一种粒子能够使石蕊溶液变成红色,某同学进行了实验探究,请填写表格中的空格,帮助该同学完成实验探究报告.
结论:稀硫酸中的H+能够使溶液变成红色.
我们仔细地对该同学的上述实验探究过程分析后会发现,其实只要做上述实验步骤中的(填序号)1,在经过分析后就可以得出正确的结论.
| 实验步骤 | 实验现象 | 分析和结论 |
| 1.在蒸馏水中加入几滴石蕊溶液. | 液体呈紫色. | 蒸馏水中有水分子,它不能使石蕊溶液变红色. |
| 2.在硫酸钠溶液中加入几滴石蕊溶液. | 液体呈紫色. | 硫酸钠溶液和稀硫酸中含有的相同硫酸根离子,它不能使石蕊溶液变红色. |
| 3.在稀盐酸中加入几滴石蕊溶液. | 溶液呈红色. | 稀硫酸和稀硫酸中含有的相同氢离子离子,它能使石蕊溶液变红色. |
我们仔细地对该同学的上述实验探究过程分析后会发现,其实只要做上述实验步骤中的(填序号)1,在经过分析后就可以得出正确的结论.
11.下列验证实验不能成功的是( )
| A. | 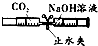 C02能与烧碱溶液反应 | B. |  不同物质的着火点不同 | ||
| C. |  分子在不断运动 | D. |  质量守恒定律 |
8.2014年12月1日全球变化大会(COP20)在秘鲁召开,其主题是“创新利用CO2,倡导低碳生活,发展低碳经济.”下列做法不符合这一主题的是( )
| A. | 开发新能源(太阳能、潮汐能、风能等),减少化石燃料的使用 | |
| B. | 限制化工发展,关停化工企业,消除污染源头 | |
| C. | 用第四代LED绿色光源代替白炽灯,节约电能 | |
| D. | 减少使用私家车次数,多乘公交车或骑自行车 |