题目内容
1.如图是配制100g质量分数为20% 的氯化钠溶液的操作过程示意图: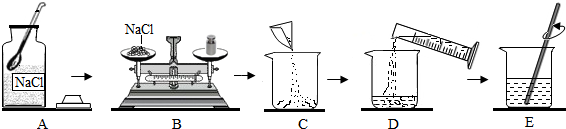
(1)计算,称量20g氯化钠
(2)D操作应选用100mL的量筒(从200mL、100mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的最低处保持水平.
(3)E操作的作用是加快氯化钠的溶解速率.
(4)若将该溶液稀释成10%的氯化钠溶液,需要加水100g应选用的仪器一组仪器是D
A.托盘天平、烧杯、玻璃棒 B.托盘天平、量筒、玻璃棒
C.烧杯、量筒、托盘天平 D.量筒、烧杯、玻璃棒.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)根据溶剂质量=溶液质量-溶质质量,计算出水的质量、体积,进而由所需水的体积判断所需量筒的量程.
(3)E操作为溶解操作,据此进行分析解答.
(4)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为20% 的氯化钠溶液,需氯化钠的质量=100g×20%=20g.
(2)溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-20g=80g(合80mL),应选用100mL的量筒.
量水时,量筒必须平放,视线要跟量筒凹液面的最低处保持水平.
(3)E操作为溶解操作,玻璃棒搅拌的作用是加快氯化钠的溶解速率.
(4)设要加水的质量为x,根据溶液稀释前后,溶质的质量不变,
则(100g+x)×10%=20g x=100g.
将该溶液稀释成10%的氯化钠溶液,应量取100g水,向盛有100g质量分数为20% 的氯化钠溶液加入100g水,用玻璃棒搅拌加快,故应选用的仪器一组仪器是量筒、烧杯、玻璃棒.
故答案为:(1)20;(2)100;最低;(3)加快氯化钠的溶解速率;(4)100;D.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器、溶质质量=溶液质量×溶质的质量分数、溶剂质量=溶液质量-溶质质量是正确解答本题的关键.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
11.用酚酞和稀硫酸的混合液在白纸上写字,要使白纸上出现红字,应喷洒的溶液是( )
| A. | 过量的氯化钠溶液 | B. | 过量的盐酸 | ||
| C. | 过量的氢氧化钠溶液 | D. | 过量的氯化钠溶液 |
12.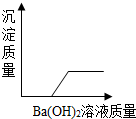 某一溶液由盐酸、碳酸钠、稀硫酸、氯化铜、氯化钠中的一种或及汇总混合而成.现向该混合溶液中滴入氢氧化钠溶液,产生的沉淀质量与加入氢氧化钠溶液体积如图所示,则下列判断正确的是( )
某一溶液由盐酸、碳酸钠、稀硫酸、氯化铜、氯化钠中的一种或及汇总混合而成.现向该混合溶液中滴入氢氧化钠溶液,产生的沉淀质量与加入氢氧化钠溶液体积如图所示,则下列判断正确的是( )
 某一溶液由盐酸、碳酸钠、稀硫酸、氯化铜、氯化钠中的一种或及汇总混合而成.现向该混合溶液中滴入氢氧化钠溶液,产生的沉淀质量与加入氢氧化钠溶液体积如图所示,则下列判断正确的是( )
某一溶液由盐酸、碳酸钠、稀硫酸、氯化铜、氯化钠中的一种或及汇总混合而成.现向该混合溶液中滴入氢氧化钠溶液,产生的沉淀质量与加入氢氧化钠溶液体积如图所示,则下列判断正确的是( )| A. | 该溶液中含有硫酸或盐酸,也可能两种酸同时含有 | |
| B. | 该溶液中不可能含碳酸钠 | |
| C. | 该溶液是否含氯化铜能确定 | |
| D. | 该溶液中含有盐酸和氯化铜 |
16.下列物质的转变,不能有一步反应实现的是( )
| A. | CO2→Na2CO3 | B. | Ca(OH)2→NaOH | C. | CuO→Cu(OH)2 | D. | MgCl2→Mg(NO3)2 |
10.人类生存离不开能源.
(1)家用燃料的更新过程如下:

①下列有关家用燃料更新的理由,正确的是BCD(填字母序号).
A.天然气属可再生能源
B.气体燃料比固体燃料利用率更高
C.减少燃烧过程中产生的污染物
D.气体燃料便于管道输送
②为了安全起见,最好在厨房安装报警器,如果报警器显示有液化气泄漏,应立即采取的措施是关闭阀门、开窗通风.(回答一至两点即可)
(2)乙醇(C2H5OH)是一种绿色燃料.将一定量的乙醇和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
下列判断正确的是AD
A.表中a的值为2.8 B.X可能是这个反应中的催化剂
C.X可能含有氢元素 D.若起始时氧气的质量是9.6g,则无X生成.
(1)家用燃料的更新过程如下:

①下列有关家用燃料更新的理由,正确的是BCD(填字母序号).
A.天然气属可再生能源
B.气体燃料比固体燃料利用率更高
C.减少燃烧过程中产生的污染物
D.气体燃料便于管道输送
②为了安全起见,最好在厨房安装报警器,如果报警器显示有液化气泄漏,应立即采取的措施是关闭阀门、开窗通风.(回答一至两点即可)
(2)乙醇(C2H5OH)是一种绿色燃料.将一定量的乙醇和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
| 物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
A.表中a的值为2.8 B.X可能是这个反应中的催化剂
C.X可能含有氢元素 D.若起始时氧气的质量是9.6g,则无X生成.

 某同学对生铁的组成进行研究,称取生铁样品46g,把一定质量分数的稀硫酸加入样品中,测得实验数据如图所示(生铁中的杂质为碳)
某同学对生铁的组成进行研究,称取生铁样品46g,把一定质量分数的稀硫酸加入样品中,测得实验数据如图所示(生铁中的杂质为碳)