题目内容
14. 九年级化学兴趣小组的同学们用K2SO4、KCI、NH4HCO3、NH4Cl四种固体,通过混合两种固体药品的办法自制“钾,氮复合肥料”,同学们制得了成分不同的“钾,氮复合肥料”,从中抽取一份作为样品探究其成分,请回答有关问题:
九年级化学兴趣小组的同学们用K2SO4、KCI、NH4HCO3、NH4Cl四种固体,通过混合两种固体药品的办法自制“钾,氮复合肥料”,同学们制得了成分不同的“钾,氮复合肥料”,从中抽取一份作为样品探究其成分,请回答有关问题:限选试剂:稀HCI,稀H2SO4,BaCI2溶液,AgNO3浴液,蒸馏水
(1)【做出猜想】
猜想1:K2SO4和NH4HCO3;猜想2:K2SO4和NH4Cl;
猜想3:KCI和NH4HCO3;猜想4:KCl和NH4Cl.
(2)【设计方案】
①甲同学提出先用AgNO3溶液确定是否含有KCl,你是否同意并说出理由:不同意,因为AgNO3也可以与NH4Cl反应生成AgCl沉淀,不能确定是否有KCl;
②乙同学提出先确定是否含有NH4HCO3,则可以选择的试剂是稀盐酸或稀硫酸.
(3)【实验探究】(提示:碳酸氢钡溶于水)
| 实验操作 | 预期现象 | 结论 |
| 步骤1:取少量样品于试管中,滴加适量的稀酸盐(或稀硫酸) | 无气泡冒出 | 猜想2成立 |
| 步骤2:另取少量样品于另一试管中,加水溶解,滴加BaCl2 | 产生白色沉淀 |
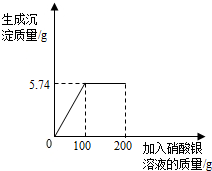
计算:硝酸银溶液中的溶质的质量分数是多少?
分析 (1)所抽样品的成分可能是KCl和 NH4HCO3,或KCl和NH4Cl,或K2SO4和 NH4HCO3,或K2SO4和NH4Cl;
(2)氯化钾、氯化铵都能够和硝酸银反应生成氯化银沉淀;
碳酸氢铵能和稀盐酸反应生成氯化铵、水和二氧化碳,能和稀硫酸反应生成硫酸铵、水和二氧化碳;
(3)氯化钾、氯化铵都不能和稀盐酸、稀硫酸、氯化钡反应;碳酸氢铵能和稀盐酸、稀硫酸反应生成二氧化碳,硫酸钾能和氯化钡反应生成硫酸钡沉淀;
(4)根据生成沉淀的质量,利用反应的化学方程式求出硝酸银的质量.
解答 解:(1)所抽样品的成分有4种可能是KCl和 NH4HCO3,也可能是KCl和NH4Cl,也可能是K2SO4和 NH4HCO3,也可能是K2SO4和NH4Cl;
(2)①不能先用AgNO3溶液确定是否含有KCl,这是因为氯化铵和硝酸银反应也能够生成白色沉淀氯化银;
②如果要先确定是否含有NH4HCO3,则可以选择的试剂是稀盐酸或稀硫酸,因为碳酸氢铵能和稀盐酸反应生成氯化铵、水和二氧化碳,能和稀硫酸反应生成硫酸铵、水和二氧化碳;
(3)实验操作1:取少量固体于试管中,滴加适量的稀盐酸或稀硫酸,不产生气泡,说明固体中不含有碳酸氢铵;
实验操作2:另取少量固体于另一支试管中,加足量的水溶解,滴加适量的氯化钡溶液,不产生沉淀,说明固体中不含有硫酸钾;
实验结论:假设2成立.
(4)设硝酸银的质量为x
KCI+AgN03═AgCl↓+KN03
170 143.5
x 5.74g
$\frac{170}{x}=\frac{143.5}{5.74g}$
x=6.8g
硝酸银溶液中硝酸银的质量分数为:$\frac{6.8g}{100g}×$100%=6.8%
答案:
(1)【做出猜想】KCl和NH4Cl
(2)【设计方案】①不同意,因为AgNO3也可以与NH4Cl反应生成AgCl沉淀,不能确定是否有KCl
②稀盐酸或稀硫酸
(3)【实验设计】
| 实验操作 | 预期现象 | 结论 |
| 步骤1:取少量样品于试管中,滴加适量的稀酸盐(或稀硫酸). | 无气泡冒出 | 猜想2成立 |
| 步骤2:另取少量样品于另一试管中,加水溶解,滴加BaCl2 | 产生白色沉淀 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

| A. | 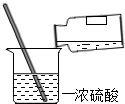 稀释浓硫酸 | B. |  向试管中加固体粉末 | ||
| C. | 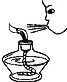 熄灭酒精灯 | D. |  过滤 |
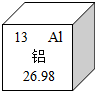 铝元素与人类关系密切.
铝元素与人类关系密切.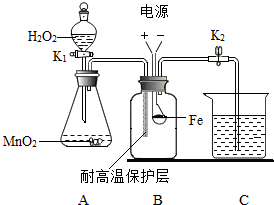 某同学用如图所示装置研究铁丝燃烧实验.
某同学用如图所示装置研究铁丝燃烧实验.