题目内容
某化学实验小组的同学利用图1装置进行常见气体的实验室制法和有关性质的研究.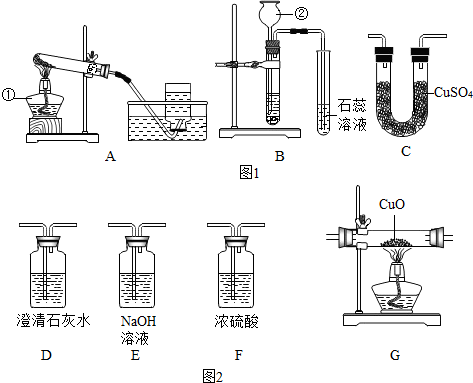
(1)写出标号仪器的名称:① ,② .
(2)甲同学选用A装置制取氧气,该反应的化学方程式是 .
(3)乙同学选用B装置制二氧化碳,并检验二氧化碳的某些性质.若选用浓盐酸和大理石制二氧化碳,该反应的化学方程式为 ,使石蕊溶液变红的酸的化学式为 .
(4)已知:水煤气中含有CO、H2、CO2、H2O;白色的硫酸铜粉末遇水变蓝.丙同学欲用图2装置证明水煤气中含有CO和H2(装置中药品均足量),应将水煤气依次通过 → → → → →尾气处理(选填字母,每个装置限用一次).

(1)写出标号仪器的名称:①
(2)甲同学选用A装置制取氧气,该反应的化学方程式是
(3)乙同学选用B装置制二氧化碳,并检验二氧化碳的某些性质.若选用浓盐酸和大理石制二氧化碳,该反应的化学方程式为
(4)已知:水煤气中含有CO、H2、CO2、H2O;白色的硫酸铜粉末遇水变蓝.丙同学欲用图2装置证明水煤气中含有CO和H2(装置中药品均足量),应将水煤气依次通过
考点:常用气体的发生装置和收集装置与选取方法,气体的净化(除杂),实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳和水反应生成碳酸;
(4)氢氧化钠能够吸收二氧化碳,浓硫酸能够吸收水蒸气,加热条件下一氧化碳和氧化铜反应生成铜和二氧化碳,氢气和氧化铜反应生成铜和水,二氧化碳能使澄清石灰水变浑浊.
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳和水反应生成碳酸;
(4)氢氧化钠能够吸收二氧化碳,浓硫酸能够吸收水蒸气,加热条件下一氧化碳和氧化铜反应生成铜和二氧化碳,氢气和氧化铜反应生成铜和水,二氧化碳能使澄清石灰水变浑浊.
解答:解:(1)①是酒精灯,常用作热源;②是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品.
故填:酒精灯;长颈漏斗.
(2)甲同学选用A装置制取氧气,试管口有一团棉花,应该是利用高锰酸钾制取氧气,该反应的化学方程式是:2KMnO4
K2MnO4+MnO2+O2↑.
故填:2KMnO4
K2MnO4+MnO2+O2↑.
(3)若选用浓盐酸和大理石制二氧化碳,该反应的化学方程式为:
CaCO3+2HCl═CaCl2+H2O+CO2↑,生成的二氧化碳进入石蕊试液中时,能和其中的水反应生成碳酸,碳酸能使石蕊试液变红色,碳酸的化学式是H2CO3.
故填:CaCO3+2HCl═CaCl2+H2O+CO2;H2CO3.
(4)已知:水煤气中含有CO、H2、CO2、H2O;白色的硫酸铜粉末遇水变蓝.欲用图2装置证明水煤气中含有CO和H2,应将水煤气依次通过装置E除去二氧化碳,再通过装置F除去水蒸气,再通过装置G使氢气、一氧化碳和氧化铜反应,再通过装置C检验生成了水,再通过装置D检验生成了二氧化碳,从而证明水煤气中含有CO和H2.
故填:E;F;G;C;D.
故填:酒精灯;长颈漏斗.
(2)甲同学选用A装置制取氧气,试管口有一团棉花,应该是利用高锰酸钾制取氧气,该反应的化学方程式是:2KMnO4
| ||
故填:2KMnO4
| ||
(3)若选用浓盐酸和大理石制二氧化碳,该反应的化学方程式为:
CaCO3+2HCl═CaCl2+H2O+CO2↑,生成的二氧化碳进入石蕊试液中时,能和其中的水反应生成碳酸,碳酸能使石蕊试液变红色,碳酸的化学式是H2CO3.
故填:CaCO3+2HCl═CaCl2+H2O+CO2;H2CO3.
(4)已知:水煤气中含有CO、H2、CO2、H2O;白色的硫酸铜粉末遇水变蓝.欲用图2装置证明水煤气中含有CO和H2,应将水煤气依次通过装置E除去二氧化碳,再通过装置F除去水蒸气,再通过装置G使氢气、一氧化碳和氧化铜反应,再通过装置C检验生成了水,再通过装置D检验生成了二氧化碳,从而证明水煤气中含有CO和H2.
故填:E;F;G;C;D.
点评:实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

练习册系列答案
相关题目
酥脆的饼干放置在空气中一段时间会变得松软,这说明空气中一定含有( )
| A、氮气 | B、氧气 | C、二氧化碳 | D、水 |


 如图是初中化学中的一些重要实验.请回答:
如图是初中化学中的一些重要实验.请回答: