��Ŀ����
5���ס��ҡ����������ֽ�������ʹ�ڸ���ʱҲ����������Ӧ���ҡ���������һ�������¶�����������Ӧ�����ε�ˮ��Һ���ñ��Ƶ�����ʢ�ţ������ֽ����Ļ����ǿ������˳���ǣ�������| A�� | �ף��ң������� | B�� | ���������ң��� | C�� | �����ң������� | D�� | �ң����������� |
���� �ڽ������˳���У�Խ��ǰ�Ľ������Խǿ��Խ���Ϳ����е�������Ӧ���پ���ֻ��ǰ��Ľ������Ժ�����������Ľ���������Һ���û�������������һ���ɿ����жϽ����Ļ��ǿ����
��� �⣺���ڼ�ʹ�ڸ���ʱҲ����������Ӧ���ҡ���������һ�������¶�����������Ӧ��˵���Ļ�ѧ���������ȶ��ģ�����������������ģ����ε�ˮ��Һ���ñ��Ƶ�����ʢ�ţ������������Ƶ�����ʢ�ţ�˵�������ܺͶ�����Һ��Ӧ�������ܹ��Ͷ�����Һ��Ӧ�������Ļ�Աȱ�ǿ�����������������ֽ����Ļ��˳�����ң����������ף�����D��ȷ��
��ѡD��
���� �����ѶȲ��Ǻܴ���Ҫ�����˽������˳���Ӧ�ã����ݷ�Ӧ�ķ������жϽ����Ļ��˳��

��ϰ��ϵ�д�
 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
�����Ŀ
2���������������ڴ�������ǣ�������
| A�� | Һ̬�� | B�� | ʯ��ʯ | C�� | ú | D�� | �����ʯ��ˮ |
20�����л�ѧ����ʽ��д��ȷ���ǣ�������
| A�� | 2P+5O2$\frac{\underline{\;��ȼ\;}}{\;}$P2O5 | B�� | 2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2�� | ||
| C�� | 2CO+O2�T2CO2 | D�� | H2O$\frac{\underline{\;ͨ��\;}}{\;}$H2+02 |
10��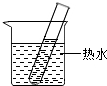 �±���KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ���ش���������
�±���KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ���ش���������
��1�������������ݣ����ɳ�KNO3���ܽ�����¶ȱ仯�Ĺ����ܽ�����¶ȵ����߶�����
��2��20��ʱ����װ��5g��KNO3������Թ��У�����10gˮ���������ʱ������ҺΪ���ͣ�ѡ����͡������͡�����Һ������Һ�����ʵ�����������24.0%������һλС�������ٽ����Թܷ���ʢ����ˮ���ձ��У�ʹ�Թ�����Һ�¶�����60�棬��ʱ�Թ��ڵ���Һ���������ܼ���������Ϊ1��2��
��3������һ����������������KNO3��Һʱ���ܽ��������Ҫ���������ձ�����������
 �±���KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ���ش���������
�±���KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ���ش���������| �¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 |
| �ܽ��/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
��2��20��ʱ����װ��5g��KNO3������Թ��У�����10gˮ���������ʱ������ҺΪ���ͣ�ѡ����͡������͡�����Һ������Һ�����ʵ�����������24.0%������һλС�������ٽ����Թܷ���ʢ����ˮ���ձ��У�ʹ�Թ�����Һ�¶�����60�棬��ʱ�Թ��ڵ���Һ���������ܼ���������Ϊ1��2��
��3������һ����������������KNO3��Һʱ���ܽ��������Ҫ���������ձ�����������
15�����л�ѧ��Ӧ�����ڷֽⷴӦ���ǣ�������
| A�� | þ+����$\stackrel{��ȼ}{��}$����þ | B�� | ʯ��+����$\stackrel{��ȼ}{��}$ˮ+������̼ | ||
| C�� | ������$\stackrel{����}{��}$��+���� | D�� | ����+����$\stackrel{����}{��}$�Ȼ��� |
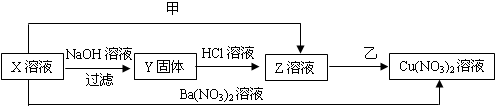
 ��A��B��C��D��E��F��G��H�Ȱ������ʣ������·�Ӧ��ϵ��ת����ϵ����Ӧ��������ʡȥ������DΪһ��ɫ��ĩ��FΪ��ɫҺ�壬H����ʹ����ʯ��ˮ����ǵ����壬E��G��Ϊ������EΪҺ�壬GΪ���壮�Իش��������⣺
��A��B��C��D��E��F��G��H�Ȱ������ʣ������·�Ӧ��ϵ��ת����ϵ����Ӧ��������ʡȥ������DΪһ��ɫ��ĩ��FΪ��ɫҺ�壬H����ʹ����ʯ��ˮ����ǵ����壬E��G��Ϊ������EΪҺ�壬GΪ���壮�Իش��������⣺