题目内容
地质考察人员发现一种带有螺纹的矿石,研究时发现该矿石能在氧气中高温煅烧,其化学反应是4X+11O2 2Fe2O3+8SO2,二氧化硫是大气主要污染物之一.下列说法不正确的是( )
2Fe2O3+8SO2,二氧化硫是大气主要污染物之一.下列说法不正确的是( )
|
| A. | X的化学式为FeS2 | B. | 该矿石是一种优质铁矿石 |
|
| C. | Fe2O3是一种黑色的固体 | D. | Fe2O3中铁元素质量分数为70% |
| 质量守恒定律及其应用;元素的质量分数计算;化学性质与物理性质的差别及应用.. | |
| 专题: | 结合课本知识的信息. |
| 分析: | A、化学反应前后,元素的种类不变,原子的种类、总个数不变; B、该矿石能在氧气中高温煅烧,其产物之一二氧化硫是大气主要污染物之一; C、Fe2O3是一种红棕色的固体; D、关键物质的化学式可以计算组成元素的质量分数. |
| 解答: | 解:A、根据反应的化学方程式4X+11O2 B、该矿石能在氧气中高温煅烧,其产物之一二氧化硫是大气主要污染物之一,该矿石不是一种优质铁矿石,该选项说法错误; C、Fe2O3是一种红棕色的固体,该选项说法错误; D、Fe2O3中铁元素的质量分数为: 故选:BC. |
| 点评: | 本题难度不大,推断物质的化学式时,要利用化学反应前后元素守恒、原子守恒来确定. |

 金钥匙试卷系列答案
金钥匙试卷系列答案
| |
 |

①该样品中碳酸钙的质量分数。(根据化学方程式列式计算)
(19)
②若取该样品10g,充分煅烧,最多可以产生CO2 (20) g。
下列关于一氧化碳的说法正确的是( )
|
| A. | 一氧化碳是无色无味无毒气体 |
|
| B. | 一氧化碳和二氧化碳的性质完全一样 |
|
| C. | 一氧化碳是具有可燃性的氧化物 |
|
| D. | 炼铁时一氧化碳与铁矿石发生了置换反应 |
钠是一种银白色固体,投入水中与水剧烈反应,熔化成闪亮小球在水面上游动,生成了氢氧化钠和氢气.下列有关钠的叙述不正确的是( )
|
| A. | 金属钠应保存在煤油中 |
|
| B. | 钠与水反应放热,使钠熔化,钠是熔点最低的金属 |
|
| C. | 金属钠的密度比水小 |
|
| D. | 钠和水反应的化学方程式为2Na+2H2O═2NaOH+H2↑ |
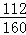 ×100%=70%,该选项说法正确.
×100%=70%,该选项说法正确.