题目内容
16.如图是部分元素原子或离子的结构示意图,请你仔细观察、分析,回答问题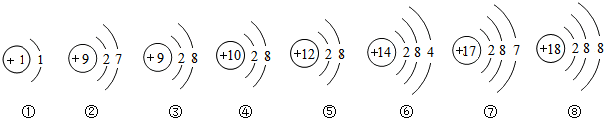
(1)上述粒子中,属于同一种元素的是②③(填序号,小同),属于阳离子的是⑤,属于阴离子的是③.
(2)⑥的元素符号用A表示,⑦的元素符号用B表示,则两者形成的化合物为AB4.
分析 (1)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同进行;当核电荷数=质子数>核外电子数,为阳子;当核电荷数=质子数<核外电子数,为阴离子,进行解答;
(2)根据结构示意图最外层电子数目的特点判断元素的化合价,由化合价写出化学式.
解答 解:(1)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同;②③的质子数相同属于同种元素;在⑤中质子数=12>核外电子数=10,为阳离子;③质子数=9<核外电子数=10,为阴离子;
(2))⑥的元素原子的最外层电子数是4,可以显+4价,⑦元素原子的最外层电子数是7,显-1价,所以则两者形成的化合物为 AB4.
故答为:(1)②③; ⑤; ③(2)AB4
点评 本题主要考查学生根据质子数与核外电子数的关系进行区别原子,离子,稀有气体的方法,并能灵活应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列推理正确的是( )
| A. | 分子是构成物质的微粒,则物质都是由分子构成的 | |
| B. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| C. | 在同一化合物中,金属元素显正价,则非金属元素一定显负价 | |
| D. | 点燃不纯的一氧化碳易发生爆炸,则点燃一氧化碳前一定要验纯 |
1.鉴别O2、CO和CO2三种无色气体,可行的简便方法是( )
| A. | 将气体分别通入澄清石灰水 | B. | 将气体分别通入石蕊试液 | ||
| C. | 试验三种气体在水中的溶解性 | D. | 将燃着的木条分别伸入三个集气瓶 |
8.兴趣小组同学发现实验台上整齐摆放的药品中(见图),有一试剂瓶的标签破损.
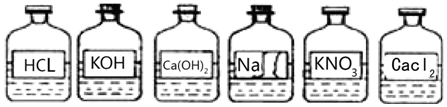
【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl溶液
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,于是他判断这是NaOH溶液.对他的操作方法、测量结果及结论的评价,正确的是B.
A.操作方法正确,结果正确,且结论正确
B.操作方法正确,结果偏小,且结论也不正确
C.操作方法不正确,结果偏大,结论不正确
D.操作方法不正确,结果正确,但结论不正确
根据实验数据,你认为一定不可能是哪个猜想(填序号),并简单阐述你的依据③,氯化钠的水溶液呈中性.
(2)要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来,他们又进行了实验,并且得到了正确的结果.请填写完成下表:
(3)小强认为还有可能是另一种溶液,请你写出溶质的化学式NaOH.

【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl溶液
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,于是他判断这是NaOH溶液.对他的操作方法、测量结果及结论的评价,正确的是B.
A.操作方法正确,结果正确,且结论正确
B.操作方法正确,结果偏小,且结论也不正确
C.操作方法不正确,结果偏大,结论不正确
D.操作方法不正确,结果正确,但结论不正确
根据实验数据,你认为一定不可能是哪个猜想(填序号),并简单阐述你的依据③,氯化钠的水溶液呈中性.
(2)要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来,他们又进行了实验,并且得到了正确的结果.请填写完成下表:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样品于试管中,加入 足量的稀盐酸 | 猜想②正确;相关的化学反应方程式: Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
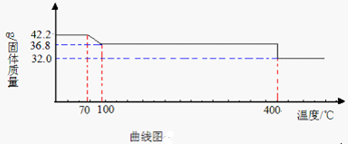
 如图所示是晓星将一定质量的铁铁粉加入到100g稀硫酸溶液中,反应进行的时间和产生的气体的质量之间的关系图象.求:(忽略气体溶解度)
如图所示是晓星将一定质量的铁铁粉加入到100g稀硫酸溶液中,反应进行的时间和产生的气体的质量之间的关系图象.求:(忽略气体溶解度)