题目内容
10.区分稀硫酸和稀盐酸,不能使用的试剂是( )| A. | 硝酸钡 | B. | 氯化钡 | C. | 氢氧化钡 | D. | 氯化钠 |
分析 根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
解答 解:A、稀硫酸能与硝酸钡溶液反应生成硫酸钡沉淀和硝酸,稀盐酸不与硝酸钡溶液反应,可以鉴别,故选项错误.
B、稀硫酸能与氯化钡溶液反应生成硫酸钡沉淀和盐酸,稀盐酸不与氯化钡溶液反应,可以鉴别,故选项错误.
C、稀硫酸能与氢氧化钡溶液反应生成硫酸钡沉淀和硝酸,稀盐酸不与氢氧化钡溶液反应,可以鉴别,故选项错误.
D、稀硫酸、稀盐酸均不氯化钠反应,不能鉴别,故选项正确.
故选:D.
点评 本题有一定难度,解答物质的鉴别题时要熟练掌握鉴别的物质的性质,然后选择适当的试剂或方法,出现不同的现象即可鉴别.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
20.水在化学实验中用途广泛,都科书下列实验图示中的水没有发生化学变化的是( )
| A. | 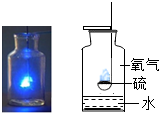 硫的燃烧 | B. | 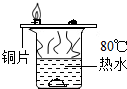 探究燃烧条件 | ||
| C. |  电解水实验 | D. | 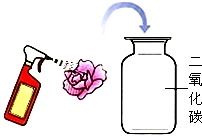 花喷水后放入CO2中 |
1.化学工业是国民经济的支柱产业.下列生产过程中,不发生化学变化的是( )
| A. |  芜湖华谊化工 | B. |  口子美酒酿造 | C. |  巢湖大理石切割 | D. |  安庆化肥生产 |
5.下列关于空气的说法错误的是( )
| A. | 空气中主要成分是氮气和氧气 | |
| B. | 空气中氧气主要来自植物的光合作用 | |
| C. | 空气中PM2.5含量高说明空气质量好 | |
| D. | 空气中的氮气可作焊接金属的保护气 |
15. 糕点疏松的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
糕点疏松的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
【探究实验一】碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液在pH试纸测上并与标准比色卡对比,读出其pH值约为10,由此得出结论是:碳酸氢钠溶液呈碱性.
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为固体溶解并产生气泡.结论:碳酸氢钠能与酸反应.
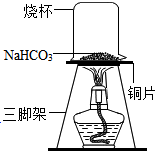
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊.
(3)通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
请分析上述操作①中不能用澄清石灰水替代氯化钙溶液的理由澄清石灰水与碳酸钠溶液反应生成氢氧化钠,不能确定固体产物是否含有氢氧化钠.
(4)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
 糕点疏松的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
糕点疏松的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.【探究实验一】碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液在pH试纸测上并与标准比色卡对比,读出其pH值约为10,由此得出结论是:碳酸氢钠溶液呈碱性.
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为固体溶解并产生气泡.结论:碳酸氢钠能与酸反应.
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊.
(3)通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量 氯化钙溶液,振荡,静置 | 产生白色沉淀 | 产物含Na2CO3 |
| ② | 取操作①后的上层清液于试管B中,滴加 酚酞试液 | 酚酞试液不变红 | 产物不含NaOH |
(4)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
7. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)小明发现燃烧产物的质量大于反应物镁条的质量,产生这一现象的原因空气中的氧气参与了反应.
(2)于是小明同学按如图装置改进了该实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2);③氮化镁可与水剧烈反应产生氮气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2;
【实验探究】请设计实验,验证猜想.
【反思与交流】空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
(3)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下.
上表中,用水进行实验的目的是对照试验.
根据上表中的实验现象,请写出两条结论,并分析可能的原因(不分析原因,不得分):①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;②温度改变反应速率,因为升高温度可以加快产生气体的速率.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)小明发现燃烧产物的质量大于反应物镁条的质量,产生这一现象的原因空气中的氧气参与了反应.
(2)于是小明同学按如图装置改进了该实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2);③氮化镁可与水剧烈反应产生氮气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2;
【实验探究】请设计实验,验证猜想.
| 实验操作 | 实验现象及结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝.证明猜想正确. |
(3)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下.
| 实验序号 | 实验1 | 实验2 | 实验3 | |
| 与镁条反应的溶液 | NH4Cl | NaCl | Na2SO4 | H2O |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡较少 |
| 加热后,实验现象 | 气泡明显增多可闻到氮味 | 气泡增多 | 气泡增多 | 气泡增多 |
根据上表中的实验现象,请写出两条结论,并分析可能的原因(不分析原因,不得分):①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;②温度改变反应速率,因为升高温度可以加快产生气体的速率.

 根据如图衣服标签回答下列问题:
根据如图衣服标签回答下列问题: