题目内容
4.根据化学方程式的计算可以从量的方面研究物质的变化.如果实际参加反应的一种反应物或生成物的质量,可以计算出其他反应物或生成物的质量.请以工业上煅烧石灰石(主要成分是CaCO3)制得生石灰(CaO)和二氧化碳的反应为例,自编一道计算题并书写在答题卡上.分析 本题为开放性题目,可以假定一种反应物或生成物的质量,计算出其他反应物或生成物的质量,注意解题格式.
解答 解:题目:工业上制取二氧化碳,是利用高温煅烧石灰石,使石灰石的主要成分碳酸钙(CaCO3)分解,制得生石灰(CaO)和二氧化碳.如果要制取5.6t氧化钙,需要碳酸钙的质量多少?
解:设需要碳酸钙的质量为x.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
x 5.6t
$\frac{100}{x}$=$\frac{56}{5.6t}$
x=10t
答:需要碳酸钙的质量为10t.(合理即可)
点评 本题主要考查有关化学方程式的计算,开放性强,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.推理是学习化学的重要思维方法,以下推理正确的是( )
| A. | 稀盐酸中能解离出氢离子,硫酸溶液中也能解离出氢离子 | |
| B. | 铝锅表面易形成致密的氧化铝薄膜耐腐蚀,铁制品表面易形成铁锈也耐腐蚀 | |
| C. | 某石灰矿中检测出含有氧化铁,因此该矿石也可用来炼铁 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
9.现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入到该烧杯中,充分反应后,测得剩余固体质量的数据记录如下:
通过计算(写出计算过程,结果精确到0.1%),求:
(1)该混合物粉末中铜的质量是4.2g.
(2)该混合物粉末中另一金属是Mg.
(3)第二次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入到该烧杯中,充分反应后,测得剩余固体质量的数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物粉末中铜的质量是4.2g.
(2)该混合物粉末中另一金属是Mg.
(3)第二次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
13.下列方框中,符合2H2意义的示意图是( )
| A. | 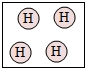 | B. | 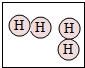 | C. | 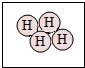 | D. | 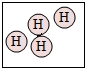 |
14.2015年3月2日,全球首批量产石墨烯手机在重庆首发.石墨烯是从石墨中分离出来的一层或几层碳原子构成的石墨片,用石墨烯与铝合金可制出一种具备特殊性能的烯合金,下列对石墨烯和烯合金的说法错误的是( )
| A. | 石墨烯在一定条件下能与氧气反应 | B. | 石墨烯在常温下化学性质活泼 | ||
| C. | 烯合金具有优良的导电性 | D. | 烯合金是一种新型材料 |