��Ŀ����
�ұ�Ϊ�ҹ���������ˮ���ұ��IJ������ݣ���ش��������⡣
(1)���ij�����ϸ�����ˮ��pH=6.6����֪ �Գ� ��(��ᡱ�)��
ͨ������Ϊˮ����һ�ֳ��������� (�ѧʽ)��
(2)��������ˮ�е���Ԫ������������ʽ���ڣ�
��3�������ӱ�ʾΪ ����Ԫ������������ʽ���ڣ��������Ļ�ѧʽΪ ��
(3)ˮ��Ӳ�Ƚϴ�ʱ����к������ǽ���Ӳ�ȵĺð취���仯ѧԭ����Ca(HCO3)2,Mg(HCO3)2���Ⱥ�����Ӧ������ˮ����Ca(HCO3)2���ȷֽ�Ϊ̼��ơ�������̼��ˮ����д����ѧ����ʽ ��Mg (HCO3)2���Ⱥ�ֽ�Ϊ������þ�Ͷ�����̼����д����ѧ����ʽ
(4)1L�ϸ����������ˮ�У�����CaCO3����Ӳ�ȣ����Ԫ�صĺ���Ӧ������ mg.

��1���ᡢH2CO3��2�֣� ��2��3Al3+��Fe2(SO4)3��4�֣�
��3��Ca(HCO3)2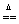 CaCO3��+H2O+CO2�� Mg(HCO3)2
CaCO3��+H2O+CO2�� Mg(HCO3)2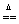 Mg(OH)2��+2CO2��(4��)
Mg(OH)2��+2CO2��(4��)
��4��180(2��)

��ϰ��ϵ�д�
�����Ŀ



 �ұ�Ϊ�ҹ���������ˮ���ұ�
�ұ�Ϊ�ҹ���������ˮ���ұ�