题目内容
10.小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的.他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动.【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:①Cr Al Cu;②Al Cr Cu.
[实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 | 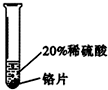 | 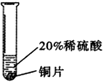 | 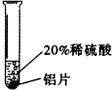 |
| 实验 现象 | 表面产生气泡缓慢,溶液变蓝色. | 无明显变化 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝与稀硫酸反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是AlCrCu | |||
②实验一发生反应的化学方程式是Cr+H2SO4═CrSO4+H2↑.
③小东提出用硫酸铜溶液代替上述实验中的稀硫酸,也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是Al、Cr都能与硫酸铜溶液发生反应.
④若实验比较铁和铜的金属活动性顺序,可选用的试剂是Fe、硫酸溶液、Cu.
分析 【实验过程】根据金属与酸或盐的反应规律,利用Al、Cr、Cu三种金属及其化合物间可发生的反应,推断Al、Cr、Cu三种金属活动性由强至弱的顺序.
【交流讨论】①根据金属的性质,分析实验前进行打磨的目的;
②根据实验一的现象及探究结果,判断实验中所发生的反应,用化学方程式表示反应;
③根据验证三种金属活动性的方案设计思路,分析实验方案不可行的原因;
④金属活动性的比较可分别利用氢前金属与酸反应时可生成氢气,氢后不能,以及活动性强的金属可以把活动性较弱的金属从其盐溶液中置换出来的规律,对铁与铜的活动性进行比较.
解答 解:【实验过程】铜不与稀硫酸反应,故现象为铜片表面无现象;由三种金属与酸反应的快慢可得出结论,铝能和稀硫酸发生反应,反应速率较快;由结论可得出三种金属在金属活动性顺序中由强到弱的相对位置关系是:Al Cr Cu;
【回答问题】(1)由于金属在保存时可能与空气中氧气发生氧化,使表面形成氧化层,影响实验,因此要使用砂纸进行打磨;
(2)由题意铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液和氢气,该反应的化学方程式为:Cr+H2SO4═CrSO4+H2↑;
(3)因为铝和铬都能与硫酸铜溶液反应,能得出铝和铬比铜活泼,但无法比较铬和铝的金属活动性强弱;
(4)铁的活动性比铜强且铁在氢前,铜在氢后,所以可利用两种金属与盐酸反应,铁与盐酸反应生成氢气,而铜不能,以及铁与硫酸铜进行反应铁可以置换出硫酸铜中的铜,利用这些原理设计实验并比较其金属活动性的大小比较.
故答案为:【实验过程】
| 实验一 | 实验二 | 实验三 | |
实验 方案 |  |  |  |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无明显变化 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝与稀硫酸反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是 Al Cr Cu | |||
(2)Cr+H2SO4═CrSO4+H2↑;
(3)Al、Cr都能与硫酸铜溶液发生反应;
(4)Fe、硫酸溶液、Cu或Fe、CuSO4等.
点评 本题考查了金属活动性顺序、有关金属活动性顺序的运用及学生的审题、综合分析能力.这里有一个知识点很重要:在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来.

 阅读快车系列答案
阅读快车系列答案| A. | 集气瓶 试管 量筒 铁架台 | |
| B. | 酒精灯 试管 蒸发皿 铁架台 | |
| C. | 集气瓶 试管 导管 铁架台 | |
| D. | 酒精灯 试管 漏斗 烧杯 |
| A. | 二氧化硫由硫元素和氧元素组成 | |
| B. | 二氧化硫分子由硫原子和氧原子组成 | |
| C. | 二氧化硫由二氧化硫分子构成 | |
| D. | 二氧化硫由硫和氧两种分子组成 |
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色.
(1)酸雨是pH小于5.6的降雨.
(2)常用脱硫方法减少废气中的SO2,以生石灰(CaO)为脱硫剂,高温下与废气中的SO2与O2化合生成CaSO4,化学方程式为2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4
(3)实验室常用亚硫酸盐与HCl或H2SO4反应制备SO2,Na2SO3与盐酸反应的化学方程式Na2SO3+2HCl═2NaCl+H2O+SO2↑.
(4)小鸿同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液的中盐成分进行如何探究:
[提出猜想]反应后的混合溶液中盐的成份是什么?
[进行猜想]
猜想1:只有K2SO3
猜想2:只有Na2SO4
猜想3:既有K2SO4,也有K2SO3
[实验探究]限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 各取2mL反应后的混合溶液分别加入A、B两只试管 | |
| 2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | 证明含有K2SO3 |
| 3 | 向B试管中,加入足量的氯化钡溶液,再加入足量的稀盐酸 | 先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有K2SO4,则猜想3成立 |