题目内容
5.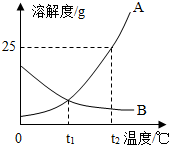 如图为A、B两种固体物质的溶解度曲线.
如图为A、B两种固体物质的溶解度曲线.(1)在t1℃时,A、B两种物质的溶解度相等.
(2)t2℃时,100g水中溶解25gA物质恰好饱和,把该饱和溶液稀释成质量分数为1 0%的溶液,应加水100g.
(3)t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是B,A、B两种物质的溶质质量分数比较A大于B(大于、小于、等于).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,在t1℃时,A、B两种物质的溶解度相等;
(2)t2℃时,A物质的溶解度是25g,所以100g水中溶解25gA物质恰好饱和,把该饱和溶液稀释成质量分数为10%的溶液,应加水$\frac{25g}{10%}$-150g=100g;
(3)A物质的溶解度随温度的升高而增大,B物质的溶解度随温度的升高而减小,所以t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,溶质的质量分数保持不变的是B,A、B两种物质的溶质质量分数比较A大于B;
故答案为:(1)t1;
(2)100;
(3)B,大于.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
15.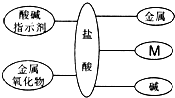 构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.
构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.
(1)图中M应为盐类物质.
(2)用盐酸除铁锈的化学方程式是Fe2O3+6HCl=2FeCl3+H2O.
(3)写出一种不能与盐酸反应的金属Cu(填化学式)
(4)将某金属投入稀盐酸中,可产生大量的无色气体.以下为该金属的部分性质,根据性质推断该金属的一种用途导线.
(5)请写出利用硝酸银检验盐酸的化学方程式AgNO3+HCl=AgCl↓+HNO3.
 构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.
构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.(1)图中M应为盐类物质.
(2)用盐酸除铁锈的化学方程式是Fe2O3+6HCl=2FeCl3+H2O.
(3)写出一种不能与盐酸反应的金属Cu(填化学式)
(4)将某金属投入稀盐酸中,可产生大量的无色气体.以下为该金属的部分性质,根据性质推断该金属的一种用途导线.
| 颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
16.二硫基丙醇是医疗上用于治疗砷中毒的药物,化学式为C3H8S2O,可进行肌肉注射或静脉注射.下列关于C3H8S2O的说法正确的是( )
| A. | 二硫基丙醇是氧化物 | |
| B. | 二硫基丙醇中氢元素的质量分数最大 | |
| C. | 二硫基丙醇中有3个碳原子 | |
| D. | 该物质中C、H、S、O原子的个数比为3:8:2:1 |
13.小明同学往氢氧化钠溶液中滴加稀盐酸研究中和反应时,忘记了滴加酸碱指示剂.为了确认滴加的盐酸是否已经过量,从烧杯中取少量反应后的溶液于试管中,用某种试剂进行检验.如表是小明同学设计的实验方案,其中错误的是( )
| 实验方案 | 使用的试剂 | 判断的方法 |
| A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
| B | 氧化铜 | 如果氧化铜溶解,溶液变蓝说明盐酸已经过量 |
| C | 酚酞 | 如果溶液仍为无色,表明盐酸已经过量 |
| D | 碳酸钠粉末 | 如果有气泡产生,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
20.红枣常食有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”.其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】①铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
②碳酸钠溶液和氢氧化钙溶液反应会生成碳酸钙沉淀,反应的方程式为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙会和水反应生成氢氧化钙.
(2)甲同学的实验中如果含有Fe2O3,则会和盐酸发生反应,Fe2O3和盐酸发生反应的方程式为①Fe2O3+6HCl═2FeCl3+3H2O,丙同学思考后认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是②氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色
他们设计如下实验方案继续验证.

乙同学对滤渣B进行探究.
【反思与评价】
(1)乙同学经过实验测得上述滤渣C的质量为1.0g,计算滤液A中含氢氧化钙的质量.(写出解题过程)
(2)丙同学经过实验测得磁铁吸引后残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g.综合上述实验及乙、丙同学的数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
(3)结合固体的成分,你认为这包“504双吸剂”,除了能吸收空气中的水分外,还能吸收空气中的氧气从而达到防腐的作用.
【提出问题】久置固体的成分是什么?
【查阅资料】①铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
②碳酸钠溶液和氢氧化钙溶液反应会生成碳酸钙沉淀,反应的方程式为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有①CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量②气泡产生,得到浅绿色溶液. | 固体中一定含有③Fe, 一定不含Fe2O3 |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙会和水反应生成氢氧化钙.
(2)甲同学的实验中如果含有Fe2O3,则会和盐酸发生反应,Fe2O3和盐酸发生反应的方程式为①Fe2O3+6HCl═2FeCl3+3H2O,丙同学思考后认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是②氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色
他们设计如下实验方案继续验证.

乙同学对滤渣B进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡冒出、溶液变为黄色溶液变为黄色、澄清的石灰水变浑浊 澄清的石灰水变浑浊 | 固体中一定含有 ③CaCO3和Fe2O3 |
(1)乙同学经过实验测得上述滤渣C的质量为1.0g,计算滤液A中含氢氧化钙的质量.(写出解题过程)
(2)丙同学经过实验测得磁铁吸引后残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g.综合上述实验及乙、丙同学的数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
(3)结合固体的成分,你认为这包“504双吸剂”,除了能吸收空气中的水分外,还能吸收空气中的氧气从而达到防腐的作用.
17.欲配制25g质量分数为10%的氯化钠溶液,下列说法不正确的是( )
| A. | 实验中用到的玻璃仪器只有烧杯和量筒 | |
| B. | 计算得氯化钠的质量为2.5g,水的体积为22.5ml | |
| C. | 量取水时,若俯视读数,会使配得的溶液浓度偏大 | |
| D. | 用天平称取该固体时将砝码和物品放反,会导致配得的溶液浓度偏小 |
14.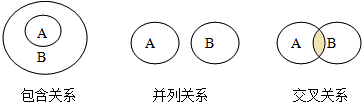 包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )
包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )
①纯净物与混合物属于包含关系;
②化合物与氧化物属于包含关系;
③单质与化合物属于交叉关系;
④金属元素与非金属元素属于并列关系;
⑤中和反应与复分解反应属于并列关系.
 包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )
包含、并列、交叉是化学概念在逻辑上存的关系(如图示),对下概念间的关系说法正确的是( )①纯净物与混合物属于包含关系;
②化合物与氧化物属于包含关系;
③单质与化合物属于交叉关系;
④金属元素与非金属元素属于并列关系;
⑤中和反应与复分解反应属于并列关系.
| A. | ①② | B. | ③④ | C. | ②④ | D. | ①⑤ |
15.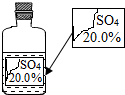 老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?
老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?
【提出猜想】老师提示:这瓶无色溶液只能是下列四种溶液中的一种:
①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铵溶液
【查阅资料】Ⅰ:(NH4)2SO4的水溶液显酸性Ⅱ:常温下,相关物质的溶解度如下:
【实验探究】
Ⅰ:通过查阅资料,小明同学认为猜想②(填序号)不成立.
Ⅱ:为确定其他几种猜想是否正确,小明同学继续进行探究:
有人认为小明实验操作第二步的结论不一定正确,他的理由是硫酸铵溶液(显酸性)也能使石蕊溶液变红.
Ⅲ:请你设计实验方案,确认该溶液是硫酸溶液并完成下列实验报告:
 老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?
老师向同学们展示了一瓶标签受损的无色溶液(如图所示)并要求同学们进行探究:确认这瓶溶液到底是什么溶液?【提出猜想】老师提示:这瓶无色溶液只能是下列四种溶液中的一种:
①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铵溶液
【查阅资料】Ⅰ:(NH4)2SO4的水溶液显酸性Ⅱ:常温下,相关物质的溶解度如下:
| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度g/100g水 | 35.1 | 19.5 | 75.4 | 与水任意比互溶 |
Ⅰ:通过查阅资料,小明同学认为猜想②(填序号)不成立.
Ⅱ:为确定其他几种猜想是否正确,小明同学继续进行探究:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步:若取该溶液少许于试管中,向其中滴加几滴 氢氧化钠溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
| 第二步:若用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟比色卡对照 | 溶液pH小于7 | 猜想③成立 |
Ⅲ:请你设计实验方案,确认该溶液是硫酸溶液并完成下列实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中,加入 锌 | 有气泡产生 | 猜想③成立,该反应的化学方程式为 Zn+H2SO4═ZnSO4+H2↑ |
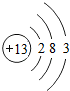 ,请回答下列问题:
,请回答下列问题:
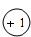 ,W离子的离子符号为Na+;
,W离子的离子符号为Na+;