题目内容
15.某兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图1),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究: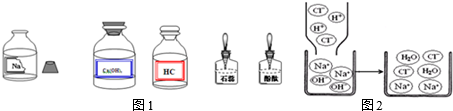
【提出问题】这瓶溶液是什么溶液?
【获得信息】实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液原来是:
猜想一:氯化钠溶液; 猜想二:氢氧化钠溶液; 猜想三:碳酸钠溶液.
【实验推断】
①甲取样滴加无色酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液,理由是氯化钠溶液呈中性,不能使无色酚酞试液变红.
②乙另取样滴加稀盐酸有气泡产生,乙得出结论:该溶液原来是碳酸钠溶液.
③丙认为乙的结论不完全正确,理由是.小组同学讨论后一致认为还需要进行如下实验:
【继续探究】④另取样加入过量的氯化钙溶液,观察到有白色沉淀产生,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色.
【得出结论】⑤这瓶溶液原来是
【拓展迁移】⑥氢氧化钠溶液与盐酸发生中和反应,恰好完全反应的微观过程如图2所示,反应的实质表达式为:H++OH-=H2O,则反应后溶液中存在的阴、阳离子是Cl-、Na+(填离子符号);请写出【继续探究】实验中加氯化钙溶液反应的实质表达式:
(仿照上例,用离子符号表示)
分析 【实验推断】①根据氯化钠、氢氧化钠、碳酸钠三种溶液的酸碱性进行分析;
②根据碳酸钠溶液与盐酸的反应进行分析;
③根据氢氧化钠与空气中二氧化碳反应进行分析;
【继续探究】根据碳酸钠和氯化钙反应结合碳酸钠和氢氧化钠的检验方法进行分析;
【实验结论】根据实验现象得出结论;
【拓展迁移】根据反应的微观示意图结合反应的实质分析.
解答 解:【实验推断】
①氢氧化钠和碳酸钠溶液都呈碱性能使酚酞试液变红色,氯化钠溶液呈中性,所以,取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液;故填:氯化钠;氯化钠溶液呈中性,不能使无色酚酞试液变红;
②若有碳酸钠存在,滴加盐酸,发生反应Na2CO3+2HCl=2NaCl+H2O+CO2↑,有气泡产生;故填:气泡;
③因为该试剂是敞口放置于空气中,若是氢氧化钠可能会和空气中二氧化碳反应变质生成部分碳酸钠,所以,丙认为乙的结论不完全正确,理由是露置于空气中的NaOH溶液与空气中的CO2反应也生成碳酸钠;故填:NaOH溶液变质后滴加稀盐酸也会产生气体;
【继续探究】要证明原来是氢氧化钠,可先加过量氯化钡或氯化钙溶液溶液除尽碳酸根,再用酚酞检验氢氧化钠的存在.所以,另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是完全除去溶液中的CO32-,避免其对OH-检验造成干扰;静置后,取上层清液,滴入酚酞试液,溶液呈红色;故填:白色沉淀;
除去Na2CO3防止干扰;
【实验结论】因为滴加氯化钙有白色沉淀产生且,滴加酚酞变红色,说明含有碳酸钠和氢氧化钠;故填:NaOH和Na2CO3;
【拓展迁移】通过观察反应的微观过程图,可以看出反应后溶液的阴阳离子为Cl-、Na+;氯化钙和碳酸钠溶液反应前存在的Ca2+、CO32-、Cl-、Na+;反应后碳酸钙是沉淀,还有离子Cl-、Na+;所以反应的实质是Ca2+和CO32-反应生成碳酸钙沉淀,即Ca2++CO32-=CaCO3↓.
故填:Cl-、Na+;Ca2++CO32-=CaCO3↓.
点评 本题是缺失标签的实验探究题,相当于物质鉴别题,在鉴别几种物质时要从物质的不同性质入手,但试题涉及知识点多,要加强知识的全面性和系统性.

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案| A. | 人体缺乏维生素A会引起坏血病 | |
| B. | 香烟的烟气中含有多种对人体有害的物质 | |
| C. | 人体缺碘或碘过量都会引起甲状腺肿大 | |
| D. | 在火场的浓烟中逃生,可用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域 |
下面是几位同学对一瓶氢氧化钠固体成分进行的探究:
探究一:确定一瓶氢氧化钠固体是否变质
小强方案:
| 实验操作 | 实验现象 | 结论 |
| 取少量样品于试管中,加入一定量水,样品全溶解后,滴加足量的稀盐酸(稀硫酸)(填一种溶液名称) | 有气泡产生 | 氢氧化钠已变质 |
小刚方案:
| 实验操作 | 实验现象 | 结论 |
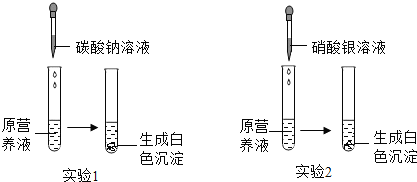
| ①取少量样品于试管中,加入一定量水后,样品全溶解后,滴加过量的CaCl2溶液 | 产生白色沉淀 | 氢氧化钠固体部分 变质 |
| ②静置后取上层清液于试管中,滴入2滴酚酞试液 | 溶液变红 |
探究三:定量分析部分变质的氢氧化钠固体中氢氧化钠的含量
1、下面是小明和小军两位同学不同的设计实验方案:
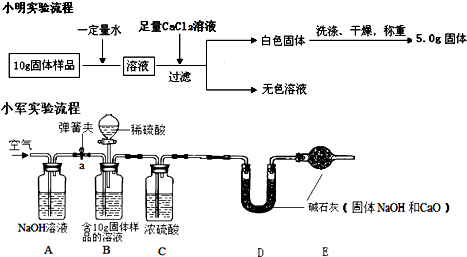
通过小明实验方案计算出样品中氢氧化钠的含量(写出计算过程)
2、小军实验步骤如下
①检查好装置气密性,装好药品后连接并固定好装置
②打开弹簧夹a,通入一段时间的空气,再称量D装置质量记录为100g
③关闭弹簧夹a,打开B装置中的分液漏斗,滴入稀硫酸,直到瓶内无气泡产生.
④打开弹簧夹a,继续通入一段时间空气,再称量D装置质量记录为102.2g
…
实验分析:
(1)在小军实验中A装置作用是除去空气中的CO2,防止其被D吸收,
(2)实验步骤④中,继续通入一段时间空气的目的是将反应生成的CO2全部排出被D吸收,
(3)如果缺装置C,最终所测得氢氧化钠的含量将会偏低(填“偏高”、“不变”、或者“偏低”)
| A. | 单质 | B. | 氧化物 | C. | 盐 | D. | 有机化合物 |
| A. | 用餐具洗洁精清洗餐具上的油污 | B. | 用汽油除去衣服上的油污 | ||
| C. | 用肥皂液洗衣 | D. | 用沐浴露洗澡 |
| A. | 降低可燃物的着火点 | B. | 增大与空气的接触面积 | ||
| C. | 提高可燃物的着火点 | D. | 增加空气中氧气含量 |
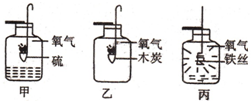
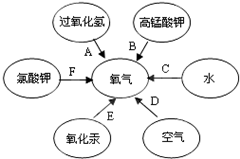 有六种途径可以制得氧气,如图所示:
有六种途径可以制得氧气,如图所示: