题目内容
6.下列各组离子在pH=1的无色溶液中一定能大量共存的是( )| A. | H+、OH-、Mg2+ | B. | Cu2+、OH-、NH4+ | C. | Na+、K+、SO42- | D. | H+、NO3-、HCO3- |
分析 pH=1的溶液中有大量的H+,大量共存要求物质之间相互交换成分不能结合生成水、气体或沉淀,形成无色溶液要求分析常见离子在水溶液中的颜色,若为无色,符合题意.
解答 解:A、H+和OH-能结合生成水,不能大量共存,故选项错误;
B、氢氧根离子和铜离子结合产生氢氧化铜沉淀,和铵根离子结合产生氨气和水,氢氧根离子和氢离子结合产生水,且Cu2+在水溶液中为蓝色,故选项错误;
C、离子之间相互交换成分不能结合生成水、气体或沉淀,且离子均为无色,故选项正确;
D、H+和HCO3-能结合生成二氧化碳和水,不能大量共存,故选项错误.
故选C.
点评 本题考查了物质能否共存的问题,溶液中的离子之间只要不会生成沉淀、气体、水中的一种,都是可以共存的,也要注意离子的带色问题.

练习册系列答案
相关题目
16.在学习碱的化学性质时,某小组同学进行了如下图实验,
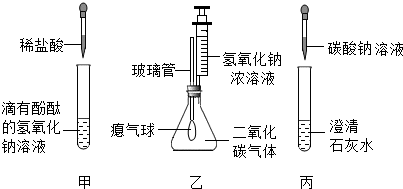
Ⅰ.探究碱的化学性质
①实验甲,随着稀盐酸的不断滴入,观察到溶液由红色变为无色;
②实验乙,滴加氢氧化钠溶液后,观察到气球变鼓
③实验丙,观察到试管内有白色沉淀产生,发生反应得化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Ⅱ.探究非也成分
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【查阅资料】BaCl2溶液呈中性且Na2CO3+BaCl2═BaCO3↓+2NaCl
【讨论交流】
①废液中一定含有的物质:碳酸钙、指示剂、水和氯化钠;
②还含有能使废液呈碱性的物质,同学们有如下猜想:
猜想1:碳酸钠;猜想2:氢氧化钠;
猜想3:氢氧化钠和碳酸钠;猜想4:氢氧化钠和氢氧化钙;
【实验设计】
同学们认为需要先验证猜想4是否成立,所需要的试剂是碳酸钠溶液,
若猜想4不成立,则需要进行后续实验,请你完成表格.
【进行实验】同学们进行实验,通过实验现象,得出了猜想2成立.

Ⅰ.探究碱的化学性质
①实验甲,随着稀盐酸的不断滴入,观察到溶液由红色变为无色;
②实验乙,滴加氢氧化钠溶液后,观察到气球变鼓
③实验丙,观察到试管内有白色沉淀产生,发生反应得化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Ⅱ.探究非也成分
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【查阅资料】BaCl2溶液呈中性且Na2CO3+BaCl2═BaCO3↓+2NaCl
【讨论交流】
①废液中一定含有的物质:碳酸钙、指示剂、水和氯化钠;
②还含有能使废液呈碱性的物质,同学们有如下猜想:
猜想1:碳酸钠;猜想2:氢氧化钠;
猜想3:氢氧化钠和碳酸钠;猜想4:氢氧化钠和氢氧化钙;
【实验设计】
同学们认为需要先验证猜想4是否成立,所需要的试剂是碳酸钠溶液,
若猜想4不成立,则需要进行后续实验,请你完成表格.
| 实验操作 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钡溶液,静置 | 有白色沉淀,溶液无色 | 猜想1正确 |
| 若没有白色沉淀,溶液呈红色 | 猜想2正确 | |
| 有白色沉淀,溶液呈红色 | 猜想3正确 |
14.下列说法中,正确的是( )
| A. | 家用电器着火,立即用水泼灭 | |
| B. | 日常生活中,用生石灰做干燥剂 | |
| C. | 发令枪中红磷燃烧时产生大量“白雾” | |
| D. | 生铁和钢都是铁合金,在用途上没有区别 |
1.下列物质中属于纯净物的是( )
| A. | 浓硫酸 | B. | 冰水 | C. | 碘酒 | D. | 稀有气体 |
18.下列有关推理中,正确的是( )
| A. | 复分解反应生成两种化合物,则生成两种化合物的反应一定是复分解反应 | |
| B. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| C. | 有机物都含碳元素,所以含碳元素的化合物一定是有机物 | |
| D. | 酸性溶液能使石蕊溶液变红,则使石蕊溶液变红的一定是酸性溶液 |
19.央视3•15晚会曝光,检测机构检验后发现市场上修正液的主要溶剂为三氯乙烷(化学式为C2H3O3).下列对三氯乙类烷的说法正确的是( )
| A. | 三氯乙烷中碳元素与氢元素的质量比为8:1 | |
| B. | 三氯乙烷的相对分子质量为133.5g | |
| C. | 三氯乙烷是无机物 | |
| D. | 三氯乙烷由4种元素组成 |