题目内容
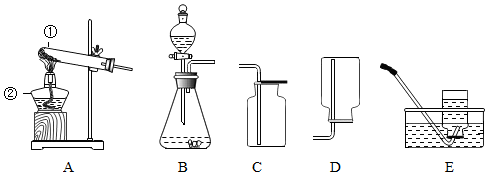
17.如图是实验室常用的制取气体的发生装置和收集装置,根据实验装置,回答问题: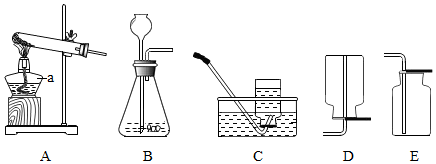
(1)有一种气体可以选用A装置制取,也可用B装置制取,该气体的化学式为O2.如果选用A与C,那么最后的两步实验操作①熄灭酒精灯 ②撤出导管,它们的操作顺序是先撤出导管,再熄灭酒精灯,这样做的目的是防止水倒流,使试管炸裂.
(2)利用提供的仪器还可以制取的另一种气体是二氧化碳,选用的制取和收集装置分别是BE.反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)如果用熟石灰粉末和碳酸氢铵固体加热就能制得氨气,氨气溶水可得到氨水.那麽你选择的制取和收集装置是AD.由此实验我们知道碳酸氢铵在给农作物施用时不能与碱性肥料混合.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.如果用熟石灰粉末和碳酸氢铵固体加热就能制得氨气,因此需要加热;氨气的密度比空气小,氨气溶水可得到氨水,因此只能用向下排空气法收集;由此实验我们知道碳酸氢铵在给农作物施用时不能与碱性肥料混合,否则会降低药效.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:O2;先撤出导管,再熄灭酒精灯;防止水倒流,使试管炸裂;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:二氧化碳;BE;CaCO3+2HCl=CaCl2+H2O+CO2↑;(合理即可)
(3)如果用熟石灰粉末和碳酸氢铵固体加热就能制得氨气,因此需要加热;氨气的密度比空气小,氨气溶水可得到氨水,因此只能用向下排空气法收集;由此实验我们知道碳酸氢铵在给农作物施用时不能与碱性肥料混合,否则会降低药效;故答案为:AD;碱性肥料;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 用量筒量取45ml水 | B. | 俯视量筒看液面 | ||
| C. | 称取5g氯化钠 | D. | 仰视量筒看液面 |
| 实验假设 | 实验内容 | 实验现象 | 实验结论 |
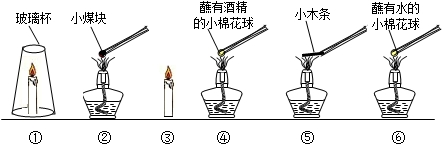
| 1.可能与物质性质有关; | [实验1]:(实验装置应选择 ④⑥;) | 燃烧;没有燃烧. | 条件1:物质具有可燃性; |
| 2.可能与是否有氧气有关; | [实验2]:(实验装置应选择 ③①;) | 很快熄灭;持续燃烧 | 条件2:要与氧气接触; |
| 3.可能与与着火点有关. | [实验3]:(实验装置应选择 ⑤②;) | 点燃时间短;点燃时间长; | 条件3:着火点低先燃烧 |
(1)原子的数目 (2)分子的数目 (3)元素的种类 (4)物质总质量(5)物质种类 (6)原子种类.
| A. | 全部 | B. | (1)(3)(4)(6) | C. | (1)(4)(6) | D. | (1)(3)(5) |