题目内容
20.白云岩矿石(含CaO、MgO)常用于生产K2SO4及氮钾复合肥.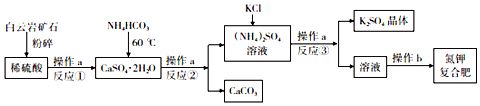
(1)将白云岩矿石粉碎的目的是增大反应物接触面积,加快反应速率;
(2)操作a是过滤;用到的玻璃仪器除玻璃棒还有烧杯和漏斗;玻璃棒的作用是引流;
(3)反应②的化学方程式为 CaSO4•2H2O+2NH4HCO3═CaCO3↓+(NH4)2SO4+CO2↑+3H2O,该反应温度需控制在60℃左右,原因:既能够加快反应速率,又能够防止碳酸氢铵分解;
(4)操作b的步骤:加热浓缩、冷却结晶、过滤而得到氮钾复合肥.
分析 (1)反应物接触面积越大,反应速率越快;
(2)过滤能够把固体和液体分离,过滤需要的玻璃仪器有烧杯、漏斗、玻璃棒等,其中玻璃棒的作用是引流;
(3)温度越高,反应速率越快,碳酸氢铵的热稳定性差,该反应温度需控制在60℃左右,既能够加快反应速率,又能够防止碳酸氢铵分解;
(4)操作b的步骤是:加热浓缩、冷却结晶、过滤而得到氮钾复合肥.
解答 解:(1)将白云岩矿石粉碎的目的是增大反应物接触面积,加快反应速率.
故填:增大反应物接触面积,加快反应速率.
(2)操作a是过滤,过滤时用到的玻璃仪器除玻璃棒还有烧杯和漏斗,其中玻璃棒的作用是引流.
故填:过滤;烧杯和漏斗;引流.
(3)反应②中,温度需控制在60℃左右,这样既能够加快反应速率,又能够防止碳酸氢铵分解.
故填:既能够加快反应速率,又能够防止碳酸氢铵分解.
(4)操作b的步骤是:加热浓缩、冷却结晶、过滤而得到氮钾复合肥.
故填:加热浓缩.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.联合国确定2017年“世界水日”的主题是“废水”,旨在引起对废水问题的关注,引导废水管理模式不断优化,下列有关“废水”的说法不正确的是( )
| A. | 硫酸工厂的酸性废水常用熟石灰中和处理后排放 | |
| B. | 印染厂的废水常含有烧碱,一般呈碱性 | |
| C. | 废水经过沉淀、过滤、吸附、消毒处理后得到的是软水 | |
| D. | 生活废水经处理达到一定标准后,可以用于浇灌农作物 |
11.推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是( )
| A. | 稀有气体可做保护气,可做保护气的一定是稀有气体 | |
| B. | 单质是由一种元素组成的物质,由一种元素组成的物质一定是单质 | |
| C. | 性质活泼的金属在空气中容易被腐蚀,铝在空气中不易被腐蚀是因为其性质不活泼 | |
| D. | PH>7的溶液使酚酞试液变红色,则使酚酞试液变红的溶液其PH>7 |
8.对下列概念的理解或相关说法中正确的是( )
| 选项 | 概念 | 解释或说法 |
| A | 置换反应 | 一定有元素化合价发生变化的反应 |
| B | 化合物 | 含有2种或2种以上元素的物质 |
| C | 中和反应 | 只要是生成盐和水的反应都是中和反应 |
| D | 离子 | 带电的微粒 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
5.下列有关水的说法中正确的是( )
| A. | 硬水通过活性炭吸附后可变为软水 | |
| B. | 水通电分解和水的蒸发都是化学变化 | |
| C. | 蒸馏水中加入肥皂水,振荡后有较多泡沫产生 | |
| D. | 水资源可以循环利用,没必要担心淡水资源不足 |
12.下列除杂方法(括号内为杂质)中正确的是( )
| A. | 一氧化碳(一氧化碳):通入氧气,点燃 | |
| B. | 碳酸钙固体(氯化钙):加入足量的水溶解,过滤、蒸发结晶 | |
| C. | 硝酸铜溶液(硝酸银):加入足量的铜粉,过滤 | |
| D. | 铁粉(氧化铜):加入适量的稀盐酸至不再产生气泡 |
9.化学与我们生活密切相关,下列有关说法中错误的是( )
| A. | 化学电池是把化学能转化为电能的装置 | |
| B. | 汽油能洗掉油污是因其具有乳化功能 | |
| C. | pH<5.6的降水属于酸雨 | |
| D. | 硝酸钾(KNO3)是一种常见的复合肥 |
10.鉴别空气、二氧化碳、氧气三瓶气体时,最简便的方法是( )
| A. | 比较三种气体的溶解性大小 | |
| B. | 测定三种气体在标准状况下的密度 | |
| C. | 将三种气体分别通入澄清的石灰水中 | |
| D. | 用燃着的木条分别伸入集气瓶内 |
