题目内容
12.(1)茶叶中含有的茶氨酸(C7H14O3N2)具有降低血压、提高记忆力、保护神经细胞、减肥等功效.请回答:①茶氨酸的类别属于有机物;
②茶氨酸中氮元素的质量分数为16.1%;(保留小数点后一位小数)
③茶氨酸中碳元素和氮元素的质量比为3:1.
(2)氢化钙(CaH2 )是一种重要的制氢剂,与水接触时,发生反应的化学方程式为:CaH2+2H2 O=Ca(OH)2+2H2↑.若需要获取40g氢气,计算至少需要氢化钙的质量.
分析 (1)①根据有机物的概念来分析;②根据化合物中某元素的质量分数的计算方法来分析;③根据化合物中元素质量比的计算方法来分析;
(2)根据40g的氢气,通过方程式列比例式计算出氢化钙的质量即可.
解答 解:(1)①含碳元素的化合物叫做有机物.由茶氨酸的化学式可知C7H14O3N2,是一种有机物;
②茶氨酸中氮元素的质量分数为:$\frac{14×2}{12×7+1×14+16×3+14×2}$×100%≈16.1%;
③茶氨酸中碳氮元素的质量比为:(12×7):(14×2)=3:1;
(2)设需要氢化钙的质量为x.
CaH2+2H2O═Ca(OH)2+2H2↑
42 4
x 40g
$\frac{42}{4}=\frac{x}{40g}$,
解得x=420g
答:需要氢化钙的质量为420g
故答案为:(1)①有机物;②16.1%;③3:1;(2)420g
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
20.向CuSO4溶液中加入一定质量的铝粉,完全反应后过滤,得滤渣和蓝色滤液.下列说法正确的是( )
| A. | 滤液中只有CuSO4 | B. | 向滤渣中滴加稀盐酸,无气泡产生 | ||
| C. | 滤液中只有Al2(SO4)3 | D. | 滤渣中一定有Cu,可能有Al |
7.金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初.以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2.下列说法不正确的是( )
| A. | 金属钛在常温下不与O2反应 | |
| B. | ②中的稀有气体的作用是隔绝空气 | |
| C. | ①中的反应TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2 | |
| D. | ②中发生的反应为置换反应 |
17.下列物质中属于混合物的是( )
| A. | 空气 | B. | 冰、水混合体 | C. | 干冰 | D. | 高锰酸钾 |
4.下列图示实验操作中,正确的是( )
| A. | 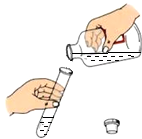 倾倒液体 | B. |  闻气味 | C. | 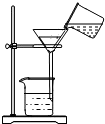 过滤 | D. | 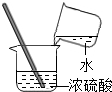 稀释浓硫酸 |
1.如图是a、b、c三种物质的溶解度曲线,据此判断,下列说法错误的是( )

| A. | t1℃时,50g水中最多能溶解10ga | |
| B. | c的溶解度变化情况与固体Ca(OH)2相似 | |
| C. | a中含有少量b时,可以用降温结晶法提纯a | |
| D. | a、c的饱和溶液从t2℃降温到t1℃时,两种溶液浓度相等 |
2.属于复分解反应的是( )
| A. | 2H2+O2 $\stackrel{点燃}{→}$2H2O | B. | CO+CuO $\stackrel{加热}{→}$ Cu+CO2 | ||
| C. | 2 KClO3 $\stackrel{加热}{→}$ 2KCl+3O2↑ | D. | Mg(OH)2+H2SO4→MgSO4+2H2O |

 已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).
已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).