题目内容
1.实验室可用水垢(主要成分是碳酸钙和氢氧化镁)制取纯净的氯化钙固体,具体制取流程如图(杂质不参与反应):
(l)操作I和操作Ⅱ的名称分别是什么?
(2)请写出加入过量的氢氧化钙时发生反应的化学方程式.
(3)第二次加入适量的稀盐酸的作用是什么?
分析 (1)根据分离混合物的方法来分析;
(2)水垢中的氢氧化镁与稀盐酸反应生成氯化镁,然后氯化镁与氢氧化钙反应;
(3)因为在上一步中加入了过量的氢氧化钙.
解答 解:(l)操作I用于分离滤渣和滤液,是过滤;操作Ⅱ是从溶液中获取晶体,属于蒸发;故填:过滤;蒸发;
(2)水垢中的氢氧化镁与稀盐酸反应生成了氯化镁,加入氢氧化钙后,氯化镁与氢氧化钙反应生成氯化钙和氢氧化镁白色沉淀;故填:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(3)在上一步中加入了过量的氢氧化钙,第二次加入适量的稀盐酸是为了除去滤液中过量的氢氧化钙;故填:为了除去滤液中过量的氢氧化钙.
点评 本题考查了混合物的分离方法、化学方程式的书写以及生产的工艺流程注意事项,难度不大.

练习册系列答案
相关题目
11.欲使一瓶pH=3的稀硫酸溶液的pH增大,下列方法不可行的是( )
| A. | 加水稀释 | B. | 加入一定量的氢氧化钠固体 | ||
| C. | 加入少量的氯化钠固体 | D. | 加入一定量的碳酸钠溶液 |
12.对下列相关事实用微观粒子的知识解释正确的是( )
| 选项 | 事 实 | 解释 |
| A | 氯化钠固体不导电 | 氯化钠固体中没有离子 |
| B | 有机物数目种类异常庞大 | 原子的排列方式不同,性质不同 |
| C | 水烧开后水壶盖容易被顶起 | 温度升高分子运动加快,体积变大 |
| D | 水结冰后不能流动 | 0℃以下,水分子不再运动 |
| A. | A | B. | B | C. | C | D. | D |
16.下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是( )
| A. | 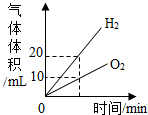 将水通电一段时间,相同状况下产生气体的体积变化 | |
| B. | 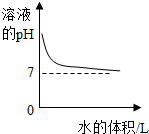 向氢氧化钠溶液中加水 | |
| C. | 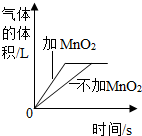 双氧水分解 | |
| D. | 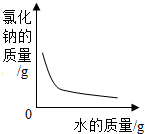 向饱和氯化钠溶液中加水稀释 |
6.蔗糖(C12H22O11)在甜菜、甘蔗中含量极高.下列有关C12H22O11的说法正确的是( )
| A. | C12H22O11属于氧化物 | |
| B. | 一个蔗糖分子中碳原子的质量为144g | |
| C. | C12H22O11中氢元素的质量分数最大 | |
| D. | C12H22O11中氢、氧原子的个数比为2:1 |
13.如图分别是铝元素、氯元素的原子结构示意图.下列叙述正确的是( )
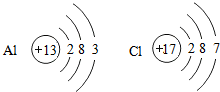

| A. | 铝原子第一电子层有3个电子 | B. | 氯原子核内有17个质子 | ||
| C. | 氯原子在化学反应中容易失去电子 | D. | 铝原子核带13个单位负电荷 |
 某固体物可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验.
某固体物可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验.