题目内容
12.实验室配制100g溶质质量分数为10%的氯化钠溶液.下列说法中错误的是( )| A. | 实验的步骤为计算、称取、量取、溶解、转移 | |
| B. | 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率 | |
| C. | 量取水时,用规格为100mL的量筒量取90mL蒸馏水 | |
| D. | 把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,贴上标签 |
分析 A、根据配制一定质量分数的溶液的步骤进行分析判断;
B、根据溶解操作中玻璃棒的作用进行分析判断;
C、利用溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,计算出配制溶液所需要的水的质量,进而由所需水的体积判断所需量筒的量程;
D、根据把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,相当于对配制的溶液进行了稀释,据此进行分析判断.
解答 解:A、实验室配制100g溶质质量分数为10%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、转移,故A正确;
B、溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率,故B正确;
C.溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为10%的氯化钠溶液,需氯化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-10g=90g(合90mL),应选用100mL的量筒,故C正确;
D.把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,相当于对配制的溶液进行了稀释,溶质的质量分数会变小,故D错误.
故选:D.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
2.物质化学式与名称(或俗称)对应的是( )
| A. | Fe(OH)2 (氢氧化铁) | B. | 氦气(He2) | C. | Na2CO3(碳酸钠) | D. | CuSO4(胆矾) |
3.关于原子、分子的叙述错误的是( )
| A. | 分子都是由原子构成的 | |
| B. | 分子和原子都在不停运动 | |
| C. | 分子和原子都是构成物质的微粒 | |
| D. | 分子和原子在化学变化中都能够再分 |
20.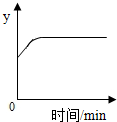 已知:Na2CO3+H2O+CO2?2NaHCO3.如图表示将二氧化碳气体缓慢通入一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2?2NaHCO3.如图表示将二氧化碳气体缓慢通入一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
 已知:Na2CO3+H2O+CO2?2NaHCO3.如图表示将二氧化碳气体缓慢通入一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )
已知:Na2CO3+H2O+CO2?2NaHCO3.如图表示将二氧化碳气体缓慢通入一定质量的碳酸钠溶液的过程中,某变量y随时间的变化趋势.纵坐标表示的是( )| A. | 溶剂的质量 | B. | 碳酸钠的质量分数 | ||
| C. | 溶液中碳元素的质量 | D. | 溶液中钠元素的质量 |
7.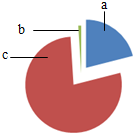 如图为空气成分示意图(按体积计算),其屮“c”代表的是( )
如图为空气成分示意图(按体积计算),其屮“c”代表的是( )
 如图为空气成分示意图(按体积计算),其屮“c”代表的是( )
如图为空气成分示意图(按体积计算),其屮“c”代表的是( )| A. | 氮气 | B. | 氧气 | C. | 稀有气体 | D. | 二氧化碳 |
17.科学家们利用太阳能产生激光使海水分解得到绿色能源---氢气,可用于化学方程式表示为2H2O$\frac{\underline{\;激光\;}}{Ti_{02}}$2H2↑+O2↑ 下列说法不正确的是( )
| A. | 水分解不产生污染物 | B. | 该技术可以将太阳能转化为氢能 | ||
| C. | TiO2在反应中作反应物 | D. | TiO2在反应中作催化剂 |
4.把20g大理石在高温加热下,充分反应至再没有气体放出为止,冷却称其剩余固体的质量(杂质不反应不挥发),相关实验数据如下:
(1)大理石属于混合物(纯净物或混合物);
(2)求大理石中碳酸钙的质量分数(写出计算过程).
| 反应前大理石质量/g | 反应后固体物质总质量/g |
| 20 | 12.08 |
(2)求大理石中碳酸钙的质量分数(写出计算过程).