题目内容
40g10%的氢氧化钠溶液与80g稀盐酸恰好完全反应,求反应后溶液中溶质的质量分数?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:稀盐酸与氢氧化钠溶液反应生成氯化钠和水;由参加反应的氢氧化钠溶液的质量、溶质的质量分数,由反应的化学方程式计算出生成氯化钠的质量,进而可计算出反应后所得溶液中溶质的质量分数.
解答:解:40g10%的氢氧化钠溶液含氢氧化钠的质量为40g×10%=4g.
设生成的氯化钠的质量为x,
HCl+NaOH=NaCl+H2O
40 58.5
4g x
=
x=5.85g
反应后溶液中溶质的质量分数为
×100%≈4.9%.
答:反应后溶液中溶质的质量分数为4.9%.
设生成的氯化钠的质量为x,
HCl+NaOH=NaCl+H2O
40 58.5
4g x
| 40 |
| 58.5 |
| 4g |
| x |
反应后溶液中溶质的质量分数为
| 5.85g |
| 40g+80g |
答:反应后溶液中溶质的质量分数为4.9%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列过程只涉及物理变化的是( )
| A、酒精挥发 | B、蜡烛燃烧 |
| C、食物腐败 | D、动物呼吸 |
现有四种粒子的结构示意图,下列说法正确的是( )
 .
.
 .
.| A、③④微粒所属元素在元素周期表中排在同一纵行 |
| B、②表示的元素在化合物中通常显2价 |
| C、②表示的是金属元素的原子 |
| D、①④表示的是阳离子 |
家庭中要除去水壶中的少量水垢(主要成分为CaCO3),采用的方法是( )
| A、用食用白醋洗涤 |
| B、用洗洁精洗涤 |
| C、用食盐水洗涤 |
| D、用淘米水洗涤 |
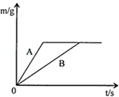 将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.
将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.