题目内容
化学学习中,我们发现很多物质之间可以相互反应,也可以相互转化。
(1)如图是盐酸与不同类别物质之间反应的知识网络。
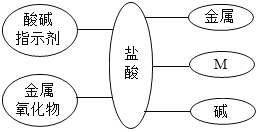
①图中M应为____________类物质。
②用盐酸除铁锈的化学方程式是______________。
③盐酸能与碱反应的实质是盐酸中的_________(写离子符号)与碱中的OH-反应生成H2O。
④现欲配制50 g质量分数10%的氢氧化钠溶液与盐酸反应,需要质量分数20%的氢氧化钠溶液________g。
(2)海水是一种重要的自然资源,利用海水可以获取许多物质,如蒸发海水可得到粗盐。粗盐中含有除氯化钠外,还含有硫酸镁、氯化钙等杂质。若按下图流程进行操作,可把粗盐提炼成精盐。

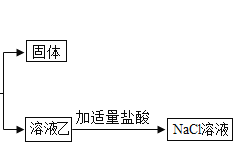
请回答:
①加入过量碳酸钠溶液的目的是__________________________。
②请设计实验,能通过清晰可见的现象,准确控制在少量溶液乙中加入稀盐酸,至恰好完全反应。___
③最后氯化钠溶液中所含的氯化钠与提纯前原粗盐水中氯化钠的质量相比较,结果_____________(选填“增大”“不变”或“减少")。
(3)某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定。取废水100g,用1%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液80g。计算废水中盐酸的溶质质量分数。__
某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的两个实验:

(1)写出 B 试管中反应的化学方程式___________;
(2)实验结束后,小组同学将 A、B 两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示), 观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成 分进行探究:
(作出猜想)
甲同学猜想:NaCl
乙同学猜想:NaCl、CaCl2、HCl
丙同学猜想:NaCl、CaCl2
丁的猜想是:_____________
(查阅资料)NaCl、CaCl2 溶液均呈中性。
(交流讨论)
甲同学认为_____________同学的猜想一定不正确,理由是:______________;
(设计实验)丙、丁两位同学分别设计如下实验验证自己的猜想:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
丙 | 取少量滤液于试管中,向其中滴加无色酚酞试液 | 无明显现象 | 猜想正确 |
丁 | 取少量滤液于试管中,向其中滴加适量稀盐酸 | _____ | 猜想正确 |
(反思评价)
实验结束后,甲同学认为_____(填“丙”或“丁”)同学的实验结论是错误的,理由是__________________。
某兴趣小组同学利用如图所示装置进行“铝与硫酸铜溶液反应”的实验时,发现反应开始后试管中出现红色固体同时产生无色无味气体。兴趣小组同学进行了以下探究。

实验1:向5份相同体积的硫酸铜溶液中分别加入表面经过打磨处理的相同长度的铝条,现象如下:
实验组别 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
硫酸铜溶液浓度 | 24% | 12% | 8% | 6% | 5% | 3% | 1% |
气泡情况 | 很快 | 快 | 较快 | 快 | 较快 | 慢 | 无 |
实验2:向质量分数为8%的硫酸铜溶液分别加入表面经过打磨处理的相同长度的铝条,现象如图所示:
实验组别 | ① | ② | ③ | ④ | ⑤ |
水浴温度(℃) | 20 | 30 | 40 | 50 | 60 |
气泡情况 | 较快 | 快 | 很快 | 很快 | 很快 |
(1)实验1的目的是______。
(2)实验2的结论是______。
(3)依据实验1和实验2,推测50℃5% 硫酸铜溶液与铝条反应的现象是______。
(反思与评价)
(4)实验2没有进行温度为70℃的实验,理由是______。
(5)根据你的猜想,气泡中的气体是______。


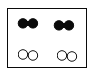 B.
B. C.
C.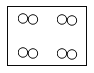 D.
D.
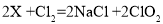 。请据此回答:以上化学方程式中,X的化学式为
。请据此回答:以上化学方程式中,X的化学式为