题目内容
18.如图是实验室常用的仪器和装置,据图回答下列问题.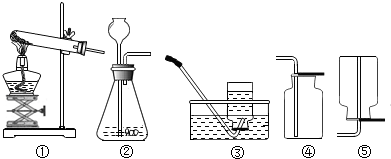
(1)实验室制取氢气的化学方程式为Zn+H2SO4═ZnSO4+H2↑,可选用的发生装置是②(填序号,下同),选择该装置的理由是反应物是固体和液体,反应在常温下发生.
(2)实验室用氯酸钾和少量二氧化锰的混合物制取氧气的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,收集装置为③.用该装置收集氧气时是否需要检验氧气已经集满?否(填“是”或“否”),需要验满时正确的操作及现象是集气瓶口处有气泡冒出(若不需要验满,只填写集满时观察到的现象)
分析 (1)实验室制取氢气常采用锌和稀硫酸来制取氢气,写出反应的化学方程式,根据药品的状态及反应条件确定发生装置;
(2)如果用氯酸钾和二氧化锰制氧气就需要加热,写出反应的化学方程式,根据药品的状态及反应条件确定发生装置,根据收集方法和氧气的性质分析验满的方法.
解答 解:(1)实验室常用锌和稀硫酸反应制取氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑,可选用的发生装置是②,选择该装置的理由是:反应物是固体和液体,反应在常温下发生.
(2)实验室用氯酸钾和少量二氧化锰的混合物制取氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;由于氧气不易溶于水,收集装置为③.用该装置收集氧气时不需要检验氧气已经集满,当集气瓶口处有气泡冒出时,说明了已收集满氧气.由于氧气的密度略大于空气,可用④装置收集,需要验满,验满的方法是:将带火星的木条伸入瓶口处,若木条复燃,则证明收集满了.
故答为:(1)Zn+H2SO4═ZnSO4+H2↑,②,反应物是固体和液体,反应在常温下发生.
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;③;否,当集气瓶口处有气泡冒出时,说明了已收集满氧气.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和过滤等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
8.生活中处处蕴含着化学知识,下列说法错误的是( )
| A. | 厨房天然气泄漏,应立即打开油烟机排气 | |
| B. | 洗涤剂去除油污是由于洗涤剂具有乳化的功能 | |
| C. | 药品中的NaHCO3可与过多胃酸反应 | |
| D. | 不可用铁质容器长期贮存食醋 |
13.下列化学方程式书写正确、符合题意且属于基本反应类型的是( )
| A. | 用火碱溶液吸收二氧化硫:SO2+2NaOH═Na2SO3+H2O | |
| B. | 植物的光合作用:6CO2+6H2O$→_{叶绿素}^{光照}$C6H12O6+6O2 | |
| C. | 碳酸饮料中碳酸的形成原理:CO2+H2O═H2CO3 | |
| D. | 利用碳的还原性得到金属铜:2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 |
10.用三块相同的铝片(均已除去氧化膜)进行如下实验.
实验1:取第一块铝片,放入稀硫酸中,有明显的现象;
实验2:取第二块铝片,放入硫酸铜溶液中,铝片表面有红色物质析出;
实验3:取第三块铝片,放入浓硫酸中,无明显的现象;
实验4:将实验3中的铝片取出,洗净后放入硫酸铜溶液中,没有明显的现象.
下列说法不正确的是( )
实验1:取第一块铝片,放入稀硫酸中,有明显的现象;
实验2:取第二块铝片,放入硫酸铜溶液中,铝片表面有红色物质析出;
实验3:取第三块铝片,放入浓硫酸中,无明显的现象;
实验4:将实验3中的铝片取出,洗净后放入硫酸铜溶液中,没有明显的现象.
下列说法不正确的是( )
| A. | 在实验1中可以观察到铝片表面有气泡产生 | |
| B. | 由实验2可以得出金属铝比铜活泼 | |
| C. | 浓硫酸与稀硫酸的化学性质有差别 | |
| D. | 铝片与浓硫酸不能发生化学反应 |
7.下列图象能正确反映对应变化关系的是( )
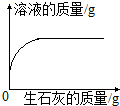 | 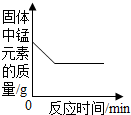 | 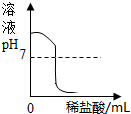 |  |
| A.一定质量的饱和石灰水中加入生石灰 | B.用酒精灯加热一定量的高锰酸钾固体 | C.向NaOH溶液中逐滴加入稀盐酸 | D.在一定量的CaCl2溶液中通入CO2气体 |
| A. | A | B. | B | C. | C | D. | D |
8. 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)依据如表数据,绘制Ca(OH)2和NaOH的溶解度曲线,上图中能表示NaOH溶解度曲线的是A(选填“A”或“B”).
(2)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到乙溶液,此时溶液中溶质的质量分数:甲>乙(选填“>”“<”或“=”).
(3)现有Ca(OH)2和NaOH两种溶质的混合溶液,若要得到较纯净的NaOH溶液,应加入适量Na2CO3溶液.
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(选填“偏大”“偏小”或“不受影响”).
 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到乙溶液,此时溶液中溶质的质量分数:甲>乙(选填“>”“<”或“=”).
(3)现有Ca(OH)2和NaOH两种溶质的混合溶液,若要得到较纯净的NaOH溶液,应加入适量Na2CO3溶液.
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(选填“偏大”“偏小”或“不受影响”).

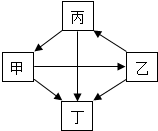 金属元素形成的化合物,依据物质的组成常见为氧化物、碱、盐,甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱,它们之间的转化关系如图(部分反应物和产物已略去,“→”表示物质间存在转化关系).请回答
金属元素形成的化合物,依据物质的组成常见为氧化物、碱、盐,甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱,它们之间的转化关系如图(部分反应物和产物已略去,“→”表示物质间存在转化关系).请回答