题目内容
1.将下列固体分别放入水中,溶液温度明显降低的是( )| A. | 烧碱 | B. | 生石灰 | C. | 硝酸铵 | D. | 食盐 |
分析 本题考查了物质溶于水时的吸、放热情况.NH4NO3溶于水时,扩散过程吸收的热量>水合过程放出的热量,说明了NH4NO3溶于水时吸收热量,溶液温度明显降低.
解答 解:烧碱、生石灰溶于水溶液的温度升高,硝酸铵溶于水溶液的温度降低,食盐溶于水温度不变.
故选C.
点评 记住典型的吸热放热的物质,例如:氢氧化钠、浓硫酸溶解放热多,温度升高(另外,氧化钙放在水中发生反应放热,也会使温度升高),溶解时表现为放热现象;硝酸铵溶解吸热多,温度降低,溶解时表现为吸热现象;其它的物质则可以认为吸热和放热相等,温度不变,表现为既不吸热,也不放热的现象.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是( )
| A. | 观察颜色 | B. | 加入澄清石灰水 | ||
| C. | 将集气瓶倒扣在水中 | D. | 将燃烧的木条伸入集气瓶中 |
16.下列数据是一些物质的pH,其中呈碱性的是( )


| A. | 牙膏 | B. | 胡萝卜 | C. | 西红柿 | D. | 食醋 |
11. NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.
NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.
查阅资料:(1)Ca(HCO3)2可溶于水
(2)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;Na2CO3的热稳定性好,受热不分解.
(3)不同温度下,Na2CO3、NaHCO3的溶解度如下表:
设计方案:为完成鉴别,同学们分别设计了自己的实验方案
(1)小芳的实验中,步骤1鉴别出来的物质是氯化钠.
(2)小明和小刚的步骤1都是溶解,该步实验的目的是鉴别碳酸钙.
进行实验:小刚在进行步骤2时,发现在两只试管中产生了白色沉淀,小刚推测它们是Na2CO3、
NaHCO3.则NaHCO3与石灰水反应的产物可能是碳酸钠、碳酸钙和水.
反思与评价:(1)小刚的设计能不能完成鉴别,理由是不能,因为他的步骤2中碳酸钠和碳酸氢钠都产生的沉淀,步骤3的目的是将碳酸钠与碳酸氢钠区别开,碳酸氢钠加热会生成二氧化碳,碳酸钠不会.
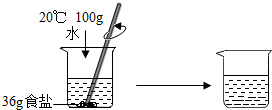
(2)小丽觉得大家的方案太麻烦,她跟老师要了一些氯化钠,做了如图所示的实验,由该实验得出的结论是20℃,100克水能溶解36克食盐.在此实验基础上,小芳用一步完成了鉴别,她的实验方法是取上述4种物质各25g,分别加入100克水溶解.
 NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.
NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料.查阅资料:(1)Ca(HCO3)2可溶于水
(2)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;Na2CO3的热稳定性好,受热不分解.
(3)不同温度下,Na2CO3、NaHCO3的溶解度如下表:
| 温度 溶解度 盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 7.0g | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 6.9g | 8.1g | 9.6g | 11.1g | 12.7g |
| 设计者 实验步骤 | 1 | 2 | 3 |
| 小芳 | 加盐酸 | 溶解 | 加热 |
| 小明 | 溶解 | 加盐酸 | 加盐酸 |
| 小刚 | 溶解 | 加石灰水 | 加热 |
(2)小明和小刚的步骤1都是溶解,该步实验的目的是鉴别碳酸钙.
进行实验:小刚在进行步骤2时,发现在两只试管中产生了白色沉淀,小刚推测它们是Na2CO3、
NaHCO3.则NaHCO3与石灰水反应的产物可能是碳酸钠、碳酸钙和水.
反思与评价:(1)小刚的设计能不能完成鉴别,理由是不能,因为他的步骤2中碳酸钠和碳酸氢钠都产生的沉淀,步骤3的目的是将碳酸钠与碳酸氢钠区别开,碳酸氢钠加热会生成二氧化碳,碳酸钠不会.
(2)小丽觉得大家的方案太麻烦,她跟老师要了一些氯化钠,做了如图所示的实验,由该实验得出的结论是20℃,100克水能溶解36克食盐.在此实验基础上,小芳用一步完成了鉴别,她的实验方法是取上述4种物质各25g,分别加入100克水溶解.
 如图是甲、乙、丙三种固体物质的溶解度曲线.在20℃时,分别将等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题
如图是甲、乙、丙三种固体物质的溶解度曲线.在20℃时,分别将等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题