题目内容
1.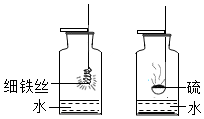 用如图装置做铁丝、硫燃烧的实验.
用如图装置做铁丝、硫燃烧的实验.(1)两瓶中都盛有少量水的原因分别是防止生成物溅落炸裂集气瓶、吸收二氧化硫,防止污染空气,两个实验共同的实验现象是燃烧都放出热量.
(2)铁丝在氧气中燃烧的实验,要绕成螺旋状的目的是增大铁丝的受热面积和氧气充分接触,有利于铁丝持续燃烧;写出铁丝燃烧的文字表达式铁+氧气$\stackrel{点燃}{→}$四氧化三铁;其反应的基本类型为化合反应.
(3)硫在空气中燃烧不如在氧气中燃烧剧烈的原因是空气中氧气浓度比纯氧中浓度低.
分析 (1)根据铁丝燃烧底部放水是为了防止生成物溅落炸裂集气瓶,硫燃烧生成二氧化硫,属于空气污染物,放入水是为了防止污染空气解答;
(2)根据铁丝在氧气中燃烧的实验的现象、注意事项、发生的反应及反应的特点进行分析解答;
(3)促进燃烧的方法有增大氧气的浓度和增大与氧气的接触面积
解答 解:(1)铁丝燃烧底部放水是为了防止生成物溅落炸裂集气瓶,硫燃烧生成二氧化硫,属于空气污染物,放入水是吸收二氧化硫,为了防止污染空气.两种物质燃烧都放出热量;
(2)铁丝要绕成螺旋状的目的是增大铁丝的受热面积和氧气充分接触,有利于铁丝持续燃烧.该反应文字表达式是:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.该反应由两种物质生成了一种物质,化学反应的类型为化合反应;
(3)硫在空气中燃烧不如在氧气中剧烈的原因是:空气中氧气浓度比纯氧中浓度低.硫燃烧是与氧气反应生成二氧化硫;
故答案为:
(1)防止生成物溅落炸裂集气瓶;吸收二氧化硫,防止污染空气;燃烧都放出热量.
(2)增大铁丝的受热面积和氧气充分接触,有利于铁丝持续燃烧;铁+氧气$\stackrel{点燃}{→}$四氧化三铁;化合反应;
(3)空气中氧气浓度比纯氧中浓度低;
点评 解答本题的关键是要充分理解铁、硫在氧气中燃烧实验的实质,只有这样才能对问题做出正确的判断.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
6.探究氯酸钾和二氧化锰制氧气实验中反应物与催化剂的最佳质量比.实验中采用如图实验装置,取20g氯酸钾,分成10等份,每份2g,分别装入10支试管中.在10支试管中分别加入不同质量的二氧化锰,分别测量二氧化锰与氯酸钾在不同质量比时,生成200mL氧气所用的时间.实验记录的数据如表所示:
请回答下列问题:
(1)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(2)此实验中收集一定体积的氧气宜采取的收集方法是排水法.原因是不易溶于水,收集气体前集气瓶内未装满水,对实验结果没有 (填“有”或“没有”)影响.
(3)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为1:3.
(4)利用双氧水和二氧化锰的混合物制氧气比加热氯酸钾和二氧化锰混合物制氧气更好.请写出前者的两个优点操作简便、节能.
(5)催化剂能影响化学反应速率,温度、反应物的浓度、接触面积等也会对化学反应速率带来影响.分析上表数据,结合影响化学反应速率的因素分析:
①当二氧化锰与氯酸钾的质量比高于最佳质量比时,反应速度变低的原因是:二氧化锰用量多,导致反应物氯酸钾的质量分数变小.
②当二氧化锰与氯酸钾的质量比低于最佳质量比时,反应速度变低的原因是:二氧化锰用量少,导致氯酸钾与二氧化锰的接触面积变小.

| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰的质量/g | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
| 二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
| 生成200mL氧气时间/秒 | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
(1)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(2)此实验中收集一定体积的氧气宜采取的收集方法是排水法.原因是不易溶于水,收集气体前集气瓶内未装满水,对实验结果没有 (填“有”或“没有”)影响.
(3)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为1:3.
(4)利用双氧水和二氧化锰的混合物制氧气比加热氯酸钾和二氧化锰混合物制氧气更好.请写出前者的两个优点操作简便、节能.
(5)催化剂能影响化学反应速率,温度、反应物的浓度、接触面积等也会对化学反应速率带来影响.分析上表数据,结合影响化学反应速率的因素分析:
①当二氧化锰与氯酸钾的质量比高于最佳质量比时,反应速度变低的原因是:二氧化锰用量多,导致反应物氯酸钾的质量分数变小.
②当二氧化锰与氯酸钾的质量比低于最佳质量比时,反应速度变低的原因是:二氧化锰用量少,导致氯酸钾与二氧化锰的接触面积变小.
10.在过氧化氢溶液制取氧气实验中用到了二氧化锰.关于二氧化锰的说法错误的是( )
| A. | 作该反应的催化剂 | B. | 反应前后其质量发生改变 | ||
| C. | 化学性质没有改变 | D. | 能加快过氧化氢的分解速率 |

 某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.
某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.