题目内容
16.人体所需的维生素C(化学式为C6H8O6)主要从蔬菜、水果中摄取.请计算:(1)维生素C中碳元素、氢元素、氧元素的质量的最简整数比为9:1:12.
(2)若要配制溶质质量分数为0.3%的维生素C溶液1000g,需要维生素C的质量为3g.
分析 (1)根据化合物中元素质量比的计算方法来分析;
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量.
解答 解:(1)维生素C中,C、H、O三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12,故填:9:1:12;
(2)配制1000g溶质质量分数为0.3%的维生素C溶液,需要维生素C的质量为1000g×0.3%=3g.
故填:3.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶剂质量=溶液质量-溶质质量是正确解答本题的关键

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
6.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 置换反应一定有单质生成,所以有单质生成的反应一定是置换反应 | |
| B. | 溶液一定具有均一性、稳定性,所以均一稳定的一定是溶液 | |
| C. | 铁能置换出硫酸铜溶液中的铜,所以铁比铜活泼 | |
| D. | 碱溶液能使无色酚酞试液变红,所以能使无色酚酞试液变红一定是碱溶液 |
1.小虎在做“盐酸中和氢氧化钠”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行了探究.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小虎对所得溶液进行了如下处理:向溶液中逐滴加入FeCl3溶液,直到不再产生沉淀为止.然后过滤,把滤液导入蒸发皿中加热,得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,请你将小虎设计的实验补充完整
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 取该溶液1-2ml与试管,滴如1-2滴无色酚酞试液,震荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性性 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小虎对所得溶液进行了如下处理:向溶液中逐滴加入FeCl3溶液,直到不再产生沉淀为止.然后过滤,把滤液导入蒸发皿中加热,得到氯化钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,请你将小虎设计的实验补充完整
| 实验操作 | 实验现象 | 结论 |
| 取样,加入碳酸钠溶液 - | 如果有气泡产生 | 溶液呈酸性 |
| 如果没有气泡产生 | 溶液呈中性 |
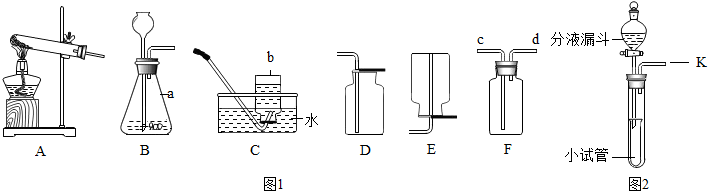
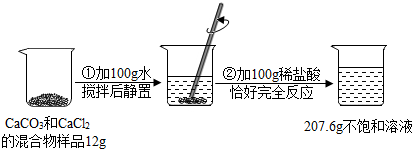
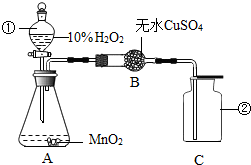 实验室中常采用分解过氧化氢溶液的方法制取氧气,某实验小组安装了如图所示的实验装置进行实验,请回答:
实验室中常采用分解过氧化氢溶液的方法制取氧气,某实验小组安装了如图所示的实验装置进行实验,请回答: