题目内容
17.置换反应是初中化学反应的基本类型之一.已知化合物A+单质B→化合物C+单质D.试回答下列问题:
(1)若D为氢气,A为稀硫酸,则B应满足的条件是在金属活动性顺序中,排在氢前面的金属.
(2)若D为铜,化合物A的化学式可能为CuO.
(3)已知在高温条件下碳与水蒸气可反应生成一氧化碳和氢气(水煤气的主要成分),写出该反应的化学方程式C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(4)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应,据此判断置换反应属于(填“属于”或“不属于”)氧化还原反应.
分析 (1)根据在金属活动性顺序中,排在氢前面的金属能和稀硫酸反应生成氢气进行解答;
(2)根据若D为铜,则化合物A为含铜元素的物质进行解答;
(3)根据高温条件下碳与水蒸气可反应生成一氧化碳和氢气进行解答;
(4)根据置换反应是单质和化合物反应生成另外的单质和化合物,所以置换反应中一定有元素的化合价的改变进行解答.
解答 解:(1)在金属活动性顺序中,排在氢前面的金属能和稀硫酸反应生成氢气;
(2)若D为铜,则化合物A为含铜元素的物质,所以化合物A的化学式可能为CuO[CuSO4、CuCl2、Cu(NO3)2均可];
(3)高温条件下碳与水蒸气可反应生成一氧化碳和氢气,该反应的化学方程式C+H2O$\frac{\underline{\;高温\;}}{\;}$ CO+H2;
(4)置换反应是单质和化合物反应生成另外的单质和化合物,所以置换反应中一定有元素的化合价的改变,所以属于氧化还原反应.
故答案为:(1)在金属活动性顺序中,排在氢前面的金属;
(2)CuO[CuSO4、CuCl2、Cu(NO3)2均可];
(3)C+H2O$\frac{\underline{\;高温\;}}{\;}$ CO+H2;
(4)属于.
点评 本题主要考查了对金属活动性顺序的应用.根据金属活动性顺序来判断反应的发生,或根据反应的发生剧烈程度判断金属的活动性强弱,从而加强学生对金属活动性顺序的理解.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
8.下列做法中,不利于节约用水的是( )
| A. | 用淘米水浇花 | B. | 用洗过衣服的水冲厕所 | ||
| C. | 将隔夜的白开水直接倒掉 | D. | 及时拧紧水龙头 |
12.打开雪碧瓶盖,会看到有气泡冒出,是因为气体的溶解度( )
| A. | 随温度升高而减小 | B. | 随温度升高而增大 | ||
| C. | 随压强减小而减小 | D. | 随压强增大而减小 |
9.下列实验方法一定能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 鉴别CO2和CO | 闻气味 |
| B | 鉴别H2和CH4 | 分别点燃,在火焰上方罩一干冷烧杯 |
| C | 鉴别石灰水和食盐水溶液 | 加入少量CO2 |
| D | 鉴别碳粉和MnO2 | 加水 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
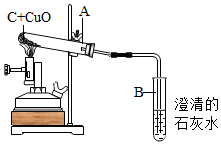 我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作为还原剂把氧化铜中的铜还原出来.
我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作为还原剂把氧化铜中的铜还原出来.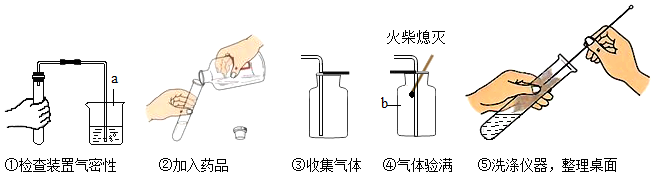
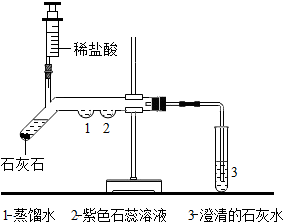
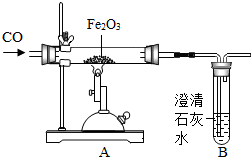 如图为“一氧化碳与氧化铁反应”的实验装置.该反应利用CO的还原性,将Fe2O3中的铁还原出来.
如图为“一氧化碳与氧化铁反应”的实验装置.该反应利用CO的还原性,将Fe2O3中的铁还原出来.