题目内容
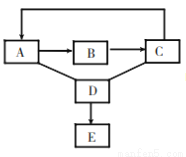
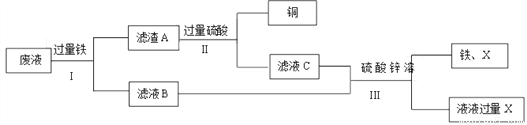
有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或 几种组成,为探究其成分,某化学兴趣小组做了如下实验,由实验现象得出的下列结论中,正确的是( )

A. 滤渣的成分为 BaSO4、CaCO3、Mg(OH)2
B. 滤液中一定含有 BaCl2 和 NaOH
C. 由实验现象可确定样品的成分
D. 生成白色沉淀的化学方程式为 BaCl2+CO2+H2O==BaCO3↓+2HCl
B 【解析】A、BaSO4不能溶于盐酸、CaCO3能与盐酸反应生成氯化钙、水和二氧化碳、Mg(OH)2能与盐酸反应生成氯化镁和水,滤渣部分溶解,产生无色气体,说明滤渣中一定存在BaSO4和CaCO3不能确定Mg(OH)2一定存在,错误;B、二氧化碳和氢氧化钠反应产生碳酸钠,碳酸钠和氯化钡反应产生的碳酸钡沉淀,滤液通入二氧化碳产生沉淀,滤液中一定含有 BaCl2 和 NaOH,正确;C、由A、...
练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目


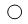 、
、 )分别表示不同元素的原子,下列对图示反应的理解中,正确的是 ( )
)分别表示不同元素的原子,下列对图示反应的理解中,正确的是 ( )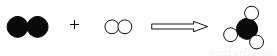
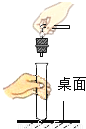 塞紧橡皮塞
塞紧橡皮塞 称取一定质量的氢氧化钠固体
称取一定质量的氢氧化钠固体 稀释浓硫酸
稀释浓硫酸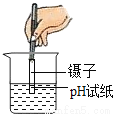 测定溶液的pH
测定溶液的pH