题目内容
6.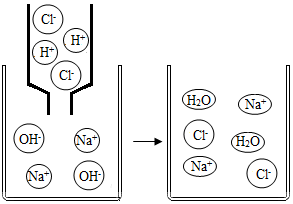 请根据氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,回答下列问题:
请根据氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,回答下列问题:(1)盐酸在水溶液中离解成H+和Cl-;
氢氧化钠在水溶液中离解成Na+和OH-;(均填写离子符号)
(2)反应后溶液中的微粒有H2O、Na+、Cl-;(填微粒符号)
(3)根据下图写出该化学反应方程式:NaOH+HCl=NaCl+H2O;
(4)以下关于该反应的说法正确的是ABCD(多选)
A.反应的实质是氢离子与氢氧根离子结合生成水
B.反应前后元素的种类没有改变
C.反应前后元素的化合价没有改变
D.反应后溶液的pH=7.
分析 因为从离子的角度分析中和反应不是教学的重点,所以此处应该视为是信息题目,要学会从给出的图分析出中和反应的本质实际上是氢离子和氢氧根离子反应生成水的过程.读图,从中或者解答题目所需要的信息,进而加工利用.
解答 解:
(1)从图中可以看出,滴入的盐酸,不是分子,而是 H+和 Cl-,所以盐酸在水溶液中离解成 H+和 Cl-;烧杯中的氢氧化钠也不是对应分子,而是自由的 Na+和 OH-,所以氢氧化钠在水溶液中离解成 Na+和 OH-;(此处要求填写离子符号)
(2)从图中可以看出,反应后溶液中的微粒有 H2O、Na+、Cl-;(此处要求填微粒符号)
(3)根据是氢氧化钠和盐酸反应生成氯化钠和水,对应的化学方程式为:NaOH+HCl=NaCl+H2O;
(4)
A.由图中可以看出,氯离子和钠离子前后没有变化,所以反应的实质是氢离子与氢氧根离子结合生成水.正确;
B.由于是化学变化,所以要遵循质量守恒定律,因此反应前后元素的种类没有改变.正确;
C.由于发生的是复分解反应,而复分解反应的特征是“两相换,价不变“,所以反应前后元素的化合价没有改变.正确;
D.由于恰好反应时,没有剩余的氢离子也没有剩余的氢氧根离子,所以反应后溶液的pH=7.正确.
故选:ABCD.
故答案为:
(1)H+; Cl-; Na+;OH-
(2)H2O、Na+、Cl-;
(3)NaOH+HCl=NaCl+H2O;
(4)ABCD.
点评 题目给出了信息图,要善于读图,从图中获取解答所需要的信息,进而分析加工.要注意答题的要求,本题前两问都书写离子符号,注意避免答非所问.

练习册系列答案
相关题目
17.下列变化不属于化学变化的是( )
| A. | 蜡烛燃烧 | B. | 海水晒盐 | C. | 钢铁锈蚀 | D. | 粮食酿酒 |
14.化学方程式是世界通用的化学语言,下列正确的化学方程式是( )
| A. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2↑+O2↑ | B. | BaCl2+Na2SO4=BaSO4↓+2NaCl | ||
| C. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | D. | 2Fe+3HCl=2FeCl3+H2↑ |
1.推理是学习化学的常见方法,以下推理合理的是( )
| A. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| B. | 有机物是指含碳元素的化合物,含碳元素的化合物一定是有机物 | |
| C. | 碱溶液能使石蕊溶液变蓝,氢氧化钾是碱,其溶液能使石蕊溶液变蓝 | |
| D. | 活泼金属与稀硫酸反应放出气体,能与稀硫酸反应放出气体的物质一定是金属 |
16.化学物质,很多是易燃、易爆、有腐蚀性或有毒的.如图所示图标不适合贴在装有鞭炮的箱子外面的是( )
| A. |  禁止烟火 | B. |  易燃物 | C. |  爆炸性 | D. |  腐蚀性 |
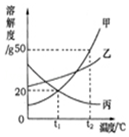 如图是甲、乙、丙三种物质的溶解度曲线.
如图是甲、乙、丙三种物质的溶解度曲线.