题目内容
11.二氧化碳和氢气可在一定条件下反应生成一种重要的化工原料甲醇,反应的化学方程式为:CO2+3H2$\frac{\underline{\;钌-膦铬合物\;}}{加压}$CH3OH+H2O.下列有关该反应的说法正确的是( )| A. | 钌-膦铬合物的质量在反应前后发生了变化 | |
| B. | 氢原子数在反应前后发生了改变 | |
| C. | 为CO2的利用创造了一种新途径 | |
| D. | 属于复分解反应 |
分析 A、二氧化碳和氢气在一定条件下反应生成甲醇和水的过程中,钌-膦铬合物作催化剂,催化剂在反应前后的质量和化学性质不变;
B、化学反应遵循质量守恒定律,即反应前后元素的种类不变,原子的总个数不变;
C、利用二氧化碳合成新物质,实现的物质的综合利用;
D、根据反应物、生成物的种类可以判断反应类型.
解答 解:A、钌-膦铬合物在反应中作催化剂,质量和化学性质不变,该选项说法不正确;
B、氢原子数在反应前后没有发生改变,该选项说法不正确;
C、利用二氧化碳合成甲醇,为二氧化碳的利用创造了一种新途径,该选项说法正确;
D、反应物是一种化合物和一种单质,不属于复分解反应,该选项说法不正确.
故选:C.
点评 二氧化碳在空气中的含量逐年增多,是造成温室效应的主要气体,实现二氧化碳的综合利用,既有利于保护环境,又有利于合成新物质,促进经济的发展.

练习册系列答案
相关题目
19.下列物质的用途,由物理性质决定的是( )
| A. | 食醋用于清除水壶中的水垢 | B. | 浓硫酸做某些气体的干燥剂 | ||
| C. | 二氧化碳作气体肥料 | D. | 用镁做军事照明弹 |
16.将等质量、等质量分数的氢氧化钠溶液和硫酸溶液混合,混合后的溶液与下列物质不能发生反应的是( )
| A. | Fe | B. | Ba(OH)2 | C. | HCl | D. | FeCl3 |
3.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )
| A. | 氢气用作燃料----氢气具有可燃性 | |
| B. | 氧化钙作食品干燥剂----氧化钙能与水反应 | |
| C. | 氮气用作保护气----氮气化学性质稳定 | |
| D. | 干冰用于人工降雨----二氧化碳能与碱反应 |
20.酸雨,是目前人类遇到的全球性区域灾难之一.煤燃烧产生的SO2气体是形成酸雨的主要污染物,原因是SO2能与水结合生成弱酸性亚硫酸(H2SO3).
【查阅资料】①H2SO3易分解生成H2O和SO2②H2SO3和SO2都能使红色的品红溶液褪色.
③H2SO3、亚硫酸盐都易与空气中的氧气或稀硝酸反应生成H2SO4、硫酸盐.
④BaSO3不溶于水,可与盐酸、硫酸反应,BaSO3与酸的反应跟CaCO3与酸反应相似.
写出BaSO3与盐酸反应的化学方程式BaSO3+2HCl=BaCl2+SO2↑+H2O.
小刚同学利用酸碱中和反应的原理,向在空气中放置一段时间的酸雨(pH约为3)中加入足量的NaOH,并就反应后混合溶液中盐的成分进行如下探究:
【提出问题】反应后的混合溶液中盐的成分是什么?
【进行猜想】猜想1:只有Na2SO3; 猜想2:只有Na2SO4; 猜想3:既有Na2SO4,也有Na2SO3.
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、石灰水、品红溶液、石蕊溶液
【反思与交流】防止酸雨保护环境可采取的有效措施有少用煤做燃料.(写出其中一条)
【查阅资料】①H2SO3易分解生成H2O和SO2②H2SO3和SO2都能使红色的品红溶液褪色.
③H2SO3、亚硫酸盐都易与空气中的氧气或稀硝酸反应生成H2SO4、硫酸盐.
④BaSO3不溶于水,可与盐酸、硫酸反应,BaSO3与酸的反应跟CaCO3与酸反应相似.
写出BaSO3与盐酸反应的化学方程式BaSO3+2HCl=BaCl2+SO2↑+H2O.
小刚同学利用酸碱中和反应的原理,向在空气中放置一段时间的酸雨(pH约为3)中加入足量的NaOH,并就反应后混合溶液中盐的成分进行如下探究:
【提出问题】反应后的混合溶液中盐的成分是什么?
【进行猜想】猜想1:只有Na2SO3; 猜想2:只有Na2SO4; 猜想3:既有Na2SO4,也有Na2SO3.
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、石灰水、品红溶液、石蕊溶液
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 分别在A、B两只试管中各加入2mL反应后的混合溶液 | |
| 2 | 向A试管中滴加几滴品红溶液,再滴入足量的稀硫酸 | 有气泡产生,品红溶液褪色, 证明含有Na2SO3. |
| 3 | 向B试管中,加入足量的氯化钡溶液 | 再加入稀盐酸 ,证明含有Na2SO4,则猜想3成立. |
1.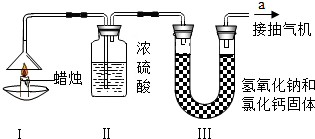 为了测定蜡烛中碳、氢元素的质量分比,同学们设计了如图的实验装置进行实验,步骤如下:先分别称量蜡烛、装置Ⅰ、装置Ⅱ的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅰ、装置Ⅲ的质量.实验数据如表.
为了测定蜡烛中碳、氢元素的质量分比,同学们设计了如图的实验装置进行实验,步骤如下:先分别称量蜡烛、装置Ⅰ、装置Ⅱ的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅰ、装置Ⅲ的质量.实验数据如表.
(1)该实验中测得水的质量为1.8gg,二氧化碳的质量为4.4gg.由该实验数据计算,蜡烛中碳、氢元素的质量之比为6:1;
(2)装置Ⅱ和装置Ⅲ的顺序能否颠倒?不能(填“能”或“不能”).
(3)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素.
(4)该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?不能(填“能”或“不能”),理由是因为空气中的水和二氧化碳也能被装置Ⅱ、装置Ⅲ吸收.
(5)装置Ⅰ利用了浓硫酸的吸水性,写出装置Ⅲ中发生的化学方程式2NaOH+CO2=Na2CO3+H2O,CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
 为了测定蜡烛中碳、氢元素的质量分比,同学们设计了如图的实验装置进行实验,步骤如下:先分别称量蜡烛、装置Ⅰ、装置Ⅱ的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅰ、装置Ⅲ的质量.实验数据如表.
为了测定蜡烛中碳、氢元素的质量分比,同学们设计了如图的实验装置进行实验,步骤如下:先分别称量蜡烛、装置Ⅰ、装置Ⅱ的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅰ、装置Ⅲ的质量.实验数据如表. | 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |
(2)装置Ⅱ和装置Ⅲ的顺序能否颠倒?不能(填“能”或“不能”).
(3)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是与消耗的蜡烛比较,生成的二氧化碳和水中增加了参加反应的氧气所含氧元素.
(4)该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?不能(填“能”或“不能”),理由是因为空气中的水和二氧化碳也能被装置Ⅱ、装置Ⅲ吸收.
(5)装置Ⅰ利用了浓硫酸的吸水性,写出装置Ⅲ中发生的化学方程式2NaOH+CO2=Na2CO3+H2O,CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.