题目内容
现有100t含氧化铁80%的赤铁矿石,工业上用于冶炼生铁
(1)生铁主要是铁和 的合金;
(2)100t含氧化铁80%的赤铁矿石中氧化铁的质量= t;
(3)用题中所给的赤铁矿石能冶炼出含杂质3%的生铁多少吨?
(反应的化学方程式为Fe2O3+3CO
2Fe+3CO2)
(1)生铁主要是铁和
(2)100t含氧化铁80%的赤铁矿石中氧化铁的质量=
(3)用题中所给的赤铁矿石能冶炼出含杂质3%的生铁多少吨?
(反应的化学方程式为Fe2O3+3CO
| ||
考点:生铁和钢,含杂质物质的化学反应的有关计算
专题:金属与金属材料
分析:(1)生铁的主要成分是铁,还有碳等杂质;
(2)根据题中信息解答;
(3)由赤铁矿的质量和氧化铁的质量分数以及生铁中杂质的质量分数,根据赤铁矿炼铁的化学方程式可以计算出炼出生铁的质量.
(2)根据题中信息解答;
(3)由赤铁矿的质量和氧化铁的质量分数以及生铁中杂质的质量分数,根据赤铁矿炼铁的化学方程式可以计算出炼出生铁的质量.
解答:解:
(1)生铁的主要成分是铁,还有碳等杂质,故生铁主要是铁和碳的合金;
(2)100t含氧化铁80%的赤铁矿石中氧化铁的质量=100t×80%=80t;
(3)设可炼出生铁的质量为x.
Fe2O3+3C
2Fe+3CO2
160 112
100t×80% x×(1-3%)
=
x≈57.7t
答:可炼出含杂质3%的生铁57.7t.
答案:
(1)碳;
(2)80t;
(3)57.73 t
(1)生铁的主要成分是铁,还有碳等杂质,故生铁主要是铁和碳的合金;
(2)100t含氧化铁80%的赤铁矿石中氧化铁的质量=100t×80%=80t;
(3)设可炼出生铁的质量为x.
Fe2O3+3C
| ||
160 112
100t×80% x×(1-3%)
| 160 |
| 112 |
| 100t |
| x×(1-3%) |
x≈57.7t
答:可炼出含杂质3%的生铁57.7t.
答案:
(1)碳;
(2)80t;
(3)57.73 t
点评:本题主要考查合金的有关概念,含杂质物质的化学方程式的计算,难度稍大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

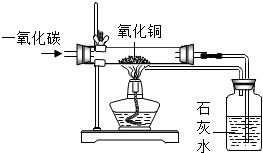 (1)如图为某同学探究CO化学性质时设计的实验装置图.下列叙述中符合如图实验设计意图的是
(1)如图为某同学探究CO化学性质时设计的实验装置图.下列叙述中符合如图实验设计意图的是
