题目内容
19.在化学实验课上,老师布置:现有铜与另一种金属R(可能是银、镁、铁中的另一种)的混合粉末,请确定R的成分.同学们设计了以下实验方案,请你一起完成: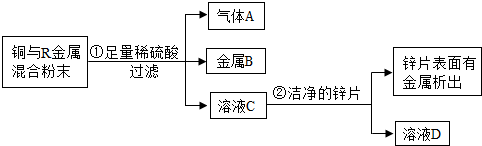
(1)请将银、镁、铁三种金属的符号填写在下列金属活动性顺序表中的相应位置.

(2)气体A是H2(写化学式),则R不可能是银(选填“银”、“镁”或“铁”).
(3)综合实验①②现象可知R是Fe,步骤②的相关化学方程式是Zn+FeSO4═ZnSO4+Fe,该反应的基本类型属于置换(选填“化合”、“分解”、“置换”或“复分解”)反应.
分析 (1)根据银、镁、铁三种金属的活动性强弱关系,判断三种金属在金属活动性顺序表中的所应处的位置.
(2)根据金属活动性顺序,排在氢前面的金属能和酸反应,后面的金属不能和酸反应分析.
(3)根据排在前面的金属能把排在后面的金属从它的盐溶液中置换出来分析.
(4)根据铜能把银置换出来,铜离子溶液是蓝色考虑实验现象,根据方程式的写法考虑方程式书写
解答 解:(1)由银、镁、铁三种金属的活动性强弱关系镁>铁>氢>银,可判断顺序表最左端空格内为镁,接下来的空格内为铁,最右端为银,如下表:
(2)由题意可知,R能与酸反应产生氢气,由金属R不可能是金属银;
(3)由于金属和酸反应产生的盐能与锌反应,可判断盐中金属活动性比锌弱,而金属镁的活动性比锌强,因此金属R应为铁;步骤②的相关化学反应是锌与生成的硫酸亚铁反应生成铁与硫酸锌.该反应的基本类型属于置换反应
故答为:(1)见上表:Mg、Fe、Ag;
(2)H2;Ag;
(3)Fe;Zn+FeSO4═ZnSO4+Fe;置换;
点评 本题属于金属活动性顺序的考查,依据金属活动性顺序中位于氢之前的金属能从酸中置换出氢,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来分析即可.

练习册系列答案
相关题目
9.下列化学用语表示正确的是( )
| A. | 两个氮原子:N2 | B. | 五氧化二磷分子:P2O5 | ||
| C. | 氢氧根离子:OH2- | D. | 碳酸钠:NaCO3 |
14.福尔马林是甲醛(化学式CH2O)的水溶液,常用作消毒剂.下列有关甲醛的说法正确的是( )
| A. | 甲醛是一种氧化物 | |
| B. | 房屋装修材料释放的甲醛对人体健康没有影响 | |
| C. | 甲醛是由一个碳原子和一个水分子构成 | |
| D. | 甲醛中碳、氢和氧三种元素的质量比为6:1:8 |
11.2013 年 3 月底,上海、安徽等地出现 H7N9 新型流感病毒,严重威胁人们健康,其治疗有效药物达菲可用莽草酸(C7H10O5)制取.有关莽草酸的说法正确的是( )
| A. | 莽草酸由碳、氢、氧三种元素组成 | |
| B. | 莽草酸中氢元素的质量分数最大 | |
| C. | 莽草酸中各元素的质量比为 7:10:5 | |
| D. | 每个莽草酸分子里含有 5 个氢分子 |
8.请根据如表回答有关问题:
(1)请在表中写出对应物质的分类(氧化物,酸,碱,盐)
(2)利用表中物质为反应物,写出符合下列要求的化学方程式:
①电解水2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
②制取氢氧化钠Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(3)若要测定纯碱溶液的酸碱度,可选用下列选项中的③
①无色酚酞试液 ②紫色石蕊试液 ③PH试纸
(4)槟榔皮上含有一种碱性物质-皂角素,皮肤沾上令人奇痒难忍,你认为可选用下列①来涂抹止痒
①食醋 ②熟石灰 ③纯碱.
| 物质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
| 分类 | 有机物 |
(2)利用表中物质为反应物,写出符合下列要求的化学方程式:
①电解水2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
②制取氢氧化钠Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(3)若要测定纯碱溶液的酸碱度,可选用下列选项中的③
①无色酚酞试液 ②紫色石蕊试液 ③PH试纸
(4)槟榔皮上含有一种碱性物质-皂角素,皮肤沾上令人奇痒难忍,你认为可选用下列①来涂抹止痒
①食醋 ②熟石灰 ③纯碱.