题目内容
17.金属材料在我们生活中起着非常重要的作用,请回答下列有关金属的问题:(1)铜丝可以用作导线,主要是因为铜具有导电性.
(2)铜、铁、铝出现的先手顺序,与金属的活动性有密切关系,只用一种溶液和金属反应验证这三种金属的活动性顺序,该溶液为B(填字母序号).
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
(3)“真金不怕火炼”的含义是金即使在高温下,也不和氧气反应.
(4)铁路建设需要大量的钢铁,在炼铁高炉中将赤铁矿还原为铁的主要化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(5)钢铁易于空气中发生锈蚀,焊接钢轨时要先除去其表面的铁锈,用稀硫酸除锈的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,金属资源不可再生,所以保护金属资源刻不容缓,除了防止金属锈蚀以外,还可采用回收利用方法(说出一种即可)
分析 (1)根据金属材料的性质和用途进行分析;
(2)根据验证三种金属的活动性顺序,常利用金属和盐溶液反应的规律来设计实验:“中间不变,两头变”、“两头不变,中间变”进行分析;
(3)根据金的性质进行分析;
(4)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳进行分析;
(5)根据氧化铁和硫酸反应生成硫酸铁和水,以及保护金属资源的途径进行分析.
解答 解:(1)铜丝可以用作导线,主要是因为铜具有导电性;
(2)验证三种金属的活动性顺序,常利用金属和盐溶液反应的规律来设计实验:“中间不变,两头变”、“两头不变,中间变”,铁、铜都不会与硫酸铝反应,不能验证,铝会与硫酸亚铁反应,铜不会与硫酸亚铁反应,可以验证三种金属的活动性顺序,铁、铝都会与硫酸铜反应,不能验证,故选:B;
(3)“真金不怕火炼”的含义是:金即使在高温下,也不和氧气反应;
(4)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(5)氧化铁和硫酸反应生成硫酸铁和水,化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,金属资源不可再生,所以保护金属资源刻不容缓,除了防止金属锈蚀以外,还可采用回收利用方法.
故答案为:(1)导电性;
(2)B;
(3)金即使在高温下,也不和氧气反应;
(4)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(5)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,回收利用.
点评 本题考查了金属的活动性顺序表以及金属与酸、金属与盐溶液反应的条件,是初中化学的重点内容,要求学生一定要牢牢的掌握,并会加以运用.

练习册系列答案
相关题目
15.氧化铜与氢氧化铜的混合物25.8g,加入稀盐酸恰好完全反应得到325.8g溶液,将滤液结晶得到40.5g的固体.稀盐酸中氢元素的质量分数为( )
| A. | 0.2% | B. | 10.3% | C. | 10.5% | D. | 10.6% |
8.下列事实和解释相符合的是( )
| A. | 洗涤剂清除油污--洗涤剂能溶解油污 | |
| B. | 汽油能清除油污--汽油具有乳化作用 | |
| C. | 清洗沼气池时严禁烟火--沼气池内有可燃性气体,遇明火可能发生爆炸 | |
| D. | 金刚石用来切割玻璃--金刚石熔点高 |
5.如图是元素周期表中铁、氧两种元素的相关信息,下列有关说法正确的是( )
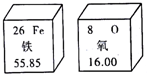

| A. | 氧原子的核外电子数为8 | |
| B. | 铁元素和氧元素都属于非金属元素 | |
| C. | 铁的相对原子质量是55.85g | |
| D. | 铁元素与氧元素只能组成一种化合物 |
12.下列物质的化学式书写正确的是( )
| A. | 碳酸钠 NaCO3 | B. | 氯化亚铁 FeCl3 | C. | 氧化镁 MgO2 | D. | 氢氧化钙 Ca(OH)2 |
9.某实验小组在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液.
(1)甲同学不小心将这两种溶液混合在一起,结果产生白色沉淀的现象,说明氢氧化钠溶液变质了.写出变质时发生反应的化学方程式2NaOH+CO2=Na2CO3+H2O.
(2)同学们对变质的氢氧化钠溶液中溶质的成分产生了兴趣,进行如下探究:
【提出问题】氢氧化钠溶液中溶质的成分是什么?
【做出猜想】猜想一:Na2CO3
猜想二:Na2CO3和NaOH(写化学式)
【进行讨论】甲同学取少量待测液加入足量的稀盐酸,有气泡产生.认为猜想一成立.乙同学不同意甲同学的观点,理由是猜想二中也含有碳酸钠,加入足量的盐酸也能产生气泡.
【设计实验】请你验证猜想二成立,并完成实验报.
【反思评价】在实验室中,氢氧化钠应密封保存.
(1)甲同学不小心将这两种溶液混合在一起,结果产生白色沉淀的现象,说明氢氧化钠溶液变质了.写出变质时发生反应的化学方程式2NaOH+CO2=Na2CO3+H2O.
(2)同学们对变质的氢氧化钠溶液中溶质的成分产生了兴趣,进行如下探究:
【提出问题】氢氧化钠溶液中溶质的成分是什么?
【做出猜想】猜想一:Na2CO3
猜想二:Na2CO3和NaOH(写化学式)
【进行讨论】甲同学取少量待测液加入足量的稀盐酸,有气泡产生.认为猜想一成立.乙同学不同意甲同学的观点,理由是猜想二中也含有碳酸钠,加入足量的盐酸也能产生气泡.
【设计实验】请你验证猜想二成立,并完成实验报.
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的待测液于试管中,加入过量的氯化钙溶液. ②充分反应后静置,取上层淸液加入无色酚酞溶液 | 产生白色沉淀 无色酚酞溶液变红 | 猜想二成立 |
6.下列物质的转化属于物理变化的是( )
| A. | 纯碱→烧碱 | B. | 生石灰→熟石灰 | C. | 石墨→金刚石 | D. | 二氧化碳→干冰 |
7.实验室部分装置如A一E图所示.
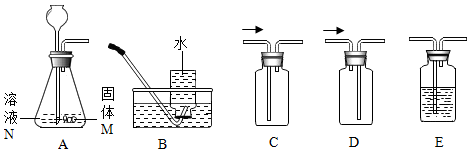
请回答下列问题:
(1)用所给装置制取并收集不同气体,填写如表空白.
(2)收集干燥的CO2还需要用装置E,E中盛装的试剂为浓硫酸.
(3)用如图装置A制取O2时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.

请回答下列问题:
(1)用所给装置制取并收集不同气体,填写如表空白.
| 固体M | 溶液N | 制取的气体 | 收集装置 |
| 大理石 | 稀盐酸 | CO2 | C |
| 二氧化锰 | 过氧化氢 | O2 | B或C |
| 锌粒 | 稀硫酸 | H2 | B或D |
(3)用如图装置A制取O2时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.


