题目内容
溶液的组成与性质
氯化氢是无色有刺激性气味的气体,能溶于乙醇,极易溶于水.已知:氯化氢溶于水得到的溶液就是我们常见的盐酸;氯化氢在干燥的乙醇中不发生电离.请回答下列问题:
(1)溶液的组成.
①在氯化氢和乙醇形成的溶液中,溶质是 ,溶剂是 ;
②组成盐酸的粒子有 .
(2)溶液的性质.
小婷同学设计了下列实验探究两种溶液的性质,请你帮她完成实验报告,填写下表的空白(假设乙醇不参加下列的反应).
(3)要测定盐酸溶液的酸碱度,可以使用的是 .
A.紫色石蕊试液 B.无色酚酞试液 C.蓝色石蕊试纸 D.pH试纸.
氯化氢是无色有刺激性气味的气体,能溶于乙醇,极易溶于水.已知:氯化氢溶于水得到的溶液就是我们常见的盐酸;氯化氢在干燥的乙醇中不发生电离.请回答下列问题:
(1)溶液的组成.
①在氯化氢和乙醇形成的溶液中,溶质是
②组成盐酸的粒子有
(2)溶液的性质.
小婷同学设计了下列实验探究两种溶液的性质,请你帮她完成实验报告,填写下表的空白(假设乙醇不参加下列的反应).
| 实验内容 | 实验现象 | 解释或化学方程式 | |
| 盐酸 | 氯化氢与乙醇的溶液 | ||
| 干燥的蓝色 石蕊试纸 | 不变色 | ||
| 锌粒 | 产生气泡 | ||
| 碳酸钠固体 | 无明显现象 | ||
A.紫色石蕊试液 B.无色酚酞试液 C.蓝色石蕊试纸 D.pH试纸.
考点:溶液的概念、组成及其特点,溶液的酸碱度测定,溶液、溶质和溶剂的相互关系与判断,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:溶液、浊液与溶解度,常见的酸 酸的通性
分析:(1)根据溶液中存在的微粒以及溶液的组成分析;
(2)根据酸的化学性质分析解答;
(3)根据溶液酸碱度的测定方法分析
(2)根据酸的化学性质分析解答;
(3)根据溶液酸碱度的测定方法分析
解答:解:(1)①在氯化氢和乙醇形成的溶液中,溶质是氯化氢,溶剂是水;
(2)盐酸能电离出氢离子,使干燥的蓝色石蕊试纸变红,而氯化氢与乙醇的溶液中氯化氢不能电离,不使干燥的蓝色石蕊试纸变红;
锌能与盐酸反应,生成氢气和氯化氢,化学方程式为:Zn+2HCl═ZnCl2+H2↑;
碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2 NaCl+H2O+CO2↑;
(3)要测定盐酸溶液的酸碱度,可以使用的是pH试纸.
故答案为:(1)①氯化氢;乙醇;
②氢离子、氯离子、水分子;
(2)溶液的性质.
(3)D
(2)盐酸能电离出氢离子,使干燥的蓝色石蕊试纸变红,而氯化氢与乙醇的溶液中氯化氢不能电离,不使干燥的蓝色石蕊试纸变红;
锌能与盐酸反应,生成氢气和氯化氢,化学方程式为:Zn+2HCl═ZnCl2+H2↑;
碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2 NaCl+H2O+CO2↑;
(3)要测定盐酸溶液的酸碱度,可以使用的是pH试纸.
故答案为:(1)①氯化氢;乙醇;
②氢离子、氯离子、水分子;
(2)溶液的性质.
| 实验内容 | 实验现象 | 解释或化学方程式 | |
| 盐酸 | 氯化氢与乙醇的溶液 | ||
| 干燥的蓝色 石蕊试纸 | 变红 | 盐酸能电离出氢离子,使干燥的蓝色石蕊试纸变红,而氯化氢与乙醇的溶液中氯化氢不能电离 | |
| 锌粒 | 无明显现象 | Zn+2HCl═ZnCl2+H2↑ | |
| 碳酸钠固体 | 有气泡产生 | Na2 CO3+2HCl═2 NaCl+H2O+CO2↑ | |
点评:本题主要考查酸的化学性质,可依据有关内容分析解答.

练习册系列答案
相关题目
下列仪器可以直接加热的一组是( )
| A、烧杯、试管 |
| B、试管、蒸发皿 |
| C、蒸发皿 锥形瓶 |
| D、锥形瓶、烧杯 |
在pH=1的无色透明液体中,能大量共存的离子组合是( )
| A、Al3+,Ag+,NO3-,Cl- |
| B、Mg2+,NH4+,NO3-,Cl- |
| C、Ca2+,Cl-,NO3-,SO42- |
| D、Ca2+,OH-,Cl-,Na+ |
下列符号只表示微观意义的是( )
| A、Cl2 |
| B、2H2 |
| C、Cu |
| D、CO2 |
下列图象能正确反映对应变化关系的是( )
A、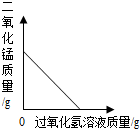 向一定量的二氧化锰中加入过氧化氢溶液 向一定量的二氧化锰中加入过氧化氢溶液 |
B、 加热一定量的高锰酸钾固体 加热一定量的高锰酸钾固体 |
C、 加热一定量的氯酸钾和二氧化锰的混合物 加热一定量的氯酸钾和二氧化锰的混合物 |
D、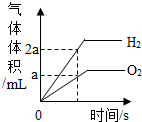 将一定质量水通电电解一段时间 将一定质量水通电电解一段时间 |
“以崇尚科学为荣,以愚昧无知为耻”.下列叙述不科学的是( )
| A、区别硬水与软水常用肥皂水 |
| B、小孩经常咬铅笔,会导致铅中毒 |
| C、加碘食盐的“碘”是指碘元素 |
| D、刚开启的地窖、窖井,不可冒然进入 |
 下面是学习了化学第二单元课题3后,进行“高锰酸钾制取氧气和氧气性质(排水法收集氧气)”的探究,请你回忆并回答下列探究内容:
下面是学习了化学第二单元课题3后,进行“高锰酸钾制取氧气和氧气性质(排水法收集氧气)”的探究,请你回忆并回答下列探究内容: