题目内容
现有一包久置的碱石灰干燥剂(主要成分CaO和NaOH),同学们用它进行了如下探究活动.[猜想与假设]该干燥剂如果发生变质,则产物可能有 (填一种).
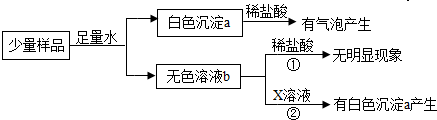
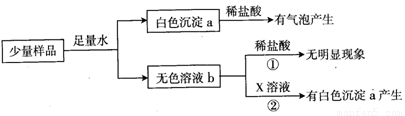
[实验与观察]
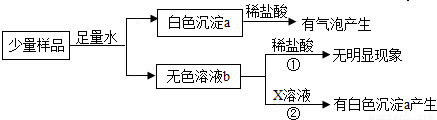
[解释与结论]白色沉淀a为 ,证明该干燥剂已经变质.由反应①可知b溶液中一定没有 ,反应②的化学方程式 ,b溶液中含有的溶质是 .
[交流与反思]关于该干燥剂的保存或使用应注意 .
【答案】分析:[猜想与假设]根据CaO和NaOH作用及与空气中的二氧化碳反应的产物分析;
[解释与结论]根据现象分析物质的种类并写出反应的方程式;
[交流与反思]根据题中碱石灰的变化进行分析.
解答:解:[猜想与假设]因为氧化钙易吸收水分变成氢氧化钙,若继续吸收二氧化碳则变成碳酸钙;氢氧化钠易吸收二氧化碳生成碳酸钠;
故产物可能有:Ca(OH)2(或CaCO3或Na2CO3);
[解释与结论]因为加水不溶解的物质是碳酸钙,故a是碳酸钙;因为反应①加稀盐酸没有明显现象,故一定没有碳酸钠;反应②中若产生白色沉淀,与钙离子有关,所以是氢氧化钙与可溶性的碳酸盐反应产生碳酸钙沉淀,故可以是:Ca(OH)2+Na2CO3═CaCO3+2NaOH;b溶液中含有的溶质是没有变质的氢氧化钠和生成的氢氧化钙;
故答案为:CaCO3;Na2CO3;Ca(OH)2+Na2CO3═CaCO3+2NaOH;NaOH和Ca(OH)2.
[交流与反思]碱石灰在空气中极易变质,所以需要密封保存;故答案为:密封保存.
点评:实验设计和猜想都要根据物质相应的性质来实施,所以应熟悉物质的性质.
[解释与结论]根据现象分析物质的种类并写出反应的方程式;
[交流与反思]根据题中碱石灰的变化进行分析.
解答:解:[猜想与假设]因为氧化钙易吸收水分变成氢氧化钙,若继续吸收二氧化碳则变成碳酸钙;氢氧化钠易吸收二氧化碳生成碳酸钠;
故产物可能有:Ca(OH)2(或CaCO3或Na2CO3);
[解释与结论]因为加水不溶解的物质是碳酸钙,故a是碳酸钙;因为反应①加稀盐酸没有明显现象,故一定没有碳酸钠;反应②中若产生白色沉淀,与钙离子有关,所以是氢氧化钙与可溶性的碳酸盐反应产生碳酸钙沉淀,故可以是:Ca(OH)2+Na2CO3═CaCO3+2NaOH;b溶液中含有的溶质是没有变质的氢氧化钠和生成的氢氧化钙;
故答案为:CaCO3;Na2CO3;Ca(OH)2+Na2CO3═CaCO3+2NaOH;NaOH和Ca(OH)2.
[交流与反思]碱石灰在空气中极易变质,所以需要密封保存;故答案为:密封保存.
点评:实验设计和猜想都要根据物质相应的性质来实施,所以应熟悉物质的性质.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目