题目内容
9.某化学兴趣小组的同学将足量镁带投入NH4CI溶液中,发现镁带逐渐溶解的同时有较多的气泡放出,镁能与NH4Cl溶液反应吗?如果能反应,生成物可能是什么?同学们进行下列实验探究:探究1:反应后所得溶液中溶质是什么?
【进行猜想】可能是MgCl2
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后溶液少量于试管中,滴入NaOH溶液 | 产生白色沉淀 | 反应后所得溶液中溶质是MgCl2 |
| 另取反应后溶液少量于试管中,滴入硝酸银和稀硝酸. |
【进行猜想】猜想一:可能是NH3;
猜想二:可能是H2;
猜想三:可能是NH3和H2的混合气体;
【查阅资料】在百度网页中输入氨气的化学性质,可以获知氨气的部分化学性质如下:
①跟谁反应:NH3+H2O═NH3•H2O
②跟酸反应:NH3+HCl═NH4Cl 2NH3+H2SO4═(NH4)2SO4
③跟某些金属氧化物反应:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2
【实验探究】为了探究气体的成分,同学们设计了如下实验装置:
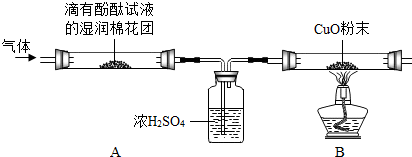
①A中观察到棉花团变红色,证明有NH3;
②B中玻璃管内观察到黑色粉末变红色,证明有H2;
③浓硫酸的作用是吸收氨气.
【实验结论】综合以上实验现象和分析,镁与NH4Cl反应的化学方程式为Mg+2NH4Cl=MgCl2+H2↑+2NH3↑.
分析 【实验验证】根据氯离子和银离子反应会生成不溶于硝酸的白色氯化银沉淀进行分析;
【进行猜想】根据质量守恒定律进行分析;
①根据氨气溶于水形成氨水,氨水能使酚酞变红色进行分析;
②根据氢气具有还原性,能使黑色的氧化铜变红色进行分析;
③根据浓硫酸是酸性干燥剂,会与碱性气体反应进行分析;
【实验结论】根据镁和氯化铵反应生成氯化镁、氢气和氨气进行分析.
解答 解:【实验验证】氯离子和银离子反应会生成不溶于硝酸的白色氯化银沉淀,所以
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后溶液少量于试管中,滴入NaOH溶液 | 产生白色沉淀 | 反应后所得溶液中溶质是MgCl2 |
| 另取反应后溶液少量于试管中,滴入硝酸银和稀硝酸 |
①氨气溶于水形成氨水,氨水能使酚酞变红色,所以A中观察到A中棉花团变红色,证明有NH3;
②氢气具有还原性,能使黑色的氧化铜变红色,所以B中玻璃管内观察到黑色粉末变红色,证明有H2;
③浓硫酸是酸性干燥剂,会与碱性气体反应,所以浓硫酸的作用是吸收氨气;
【实验结论】镁和氯化铵反应生成氯化镁、氢气和氨气,化学方程式为:Mg+2NH4Cl=MgCl2+H2↑+2NH3↑.
故答案为:【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| 硝酸银和稀硝酸 |
①棉花团变红色;
②黑色粉末变红色;
③吸收氨气;
【实验结论】Mg+2NH4Cl=MgCl2+H2↑+2NH3↑.
点评 在解此类题时,首选分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

练习册系列答案
相关题目
19.下列实验操作,正确的是( )
| A. | 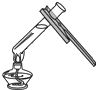 加热液体 | B. |  取用固体 | C. |  验满氧气 | D. | 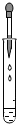 滴加液体 |
17.下列有关物质的用法有害健康的是( )
| A. | 碘酸钾加碘于食盐 | B. | 甲醛浸泡海产品保鲜 | ||
| C. | 氮气用于粮库保质 | D. | 小苏打用于糕点发酵 |
14.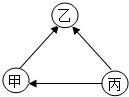 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由强到若的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由强到若的顺序是( )
 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由强到若的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由强到若的顺序是( )| A. | 乙、甲、丙 | B. | 乙、丙、甲 | C. | 丙、甲、乙 | D. | 丙、乙、甲 |
1. 构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )
构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )
 构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )
构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )| A. | 该有机物的化学式为C8H7O3 | |
| B. | 该有机物中碳、氢、氧的质量比为8:8:3 | |
| C. | 与分子模型相比,化学式不能表示分子中原子的排列方式,因此,分子模型比化学式更有推广价值 | |
| D. | 该有机物完全燃烧生成二氧化碳和水 |
19.如图所示各组转化中,一定条件下均能一步实现的组合是( )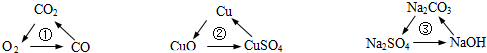

| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |

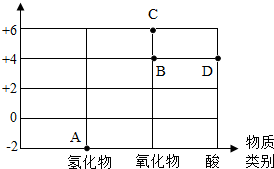 碳、氧、硫(C、O、S) 等元素在不同化合物(如坐标中的A-D物质)中化合价不同,其性质也不同.
碳、氧、硫(C、O、S) 等元素在不同化合物(如坐标中的A-D物质)中化合价不同,其性质也不同.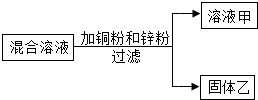 某化学小组向一定量AgNO3和Al(NO3)3的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2;②固体乙中一定含有Ag,可能含有Cu和Zn;③若溶液甲是蓝色,则溶液甲一定含Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④向固体乙滴加稀盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2,上述四种说法正确的个数为( )
某化学小组向一定量AgNO3和Al(NO3)3的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2;②固体乙中一定含有Ag,可能含有Cu和Zn;③若溶液甲是蓝色,则溶液甲一定含Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④向固体乙滴加稀盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2,上述四种说法正确的个数为( )