题目内容
11.浙江一电石厂发生火灾,电石的化学名称是碳化钙(CaC2),不可燃,是一种有机合成化学工业的基本原料,化学性质非常活泼,遇水后能激烈分解产生可燃性气体乙炔(C2H2)和一种碱,释放出大量的热.请用你学过的知识回答以下问题:(1)请写出碳化钙遇水后的化学方程式CaC2+2H2O=C2H2↑+Ca(OH)2.
(2)天津滨海新区危化品爆炸也是由于用水灭火时,水浇在了电石上引起的,请你从燃烧的条件来分析一下电石起火爆炸的原因:反应生成可燃性气体,且该反应放热,达到了可燃性气体的着火点,急速的燃烧发生在有限的空间内引起气体体积迅速膨胀而发生爆炸.
分析 (1)根据碳化钙(CaC2)和水反应生成乙炔(C2H2)气体和氢氧化钙,写出反应的方程式;
(2)根据燃烧的条件解答.
解答 解:(1)碳化钙(CaC2)和水反应生成乙炔(C2H2)气体和氢氧化钙,反应的方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2
(2)电石主要成分碳化钙(CaC2)能与水反应生成可燃性气体,且该反应放热;
答案:
(1)CaC2+2H2O=C2H2+Ca(OH)2
(2)电石主要成分碳化钙(CaC2)能与水反应生成可燃性气体,且该反应放热,达到了可燃性气体的着火点,急速的燃烧发生在有限的空间内引起气体体积迅速膨胀而发生爆炸.故填:反应生成可燃性气体,且该反应放热,达到了可燃性气体的着火点,急速的燃烧发生在有限的空间内引起气体体积迅速膨胀而发生爆炸.
点评 本题属于信息题的考查,可以依据题目提供的信息结合碳化钙(CaC2)能与水反应生成可燃性气体等相关的知识进行分析得出结论,难度不大.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
1.下列关于纯净水的叙述中错误的是( )
| A. | 能溶解高锰酸钾形成一种紫色溶液 | B. | 是无色透明的液体 | ||
| C. | 能溶解所有的物质 | D. | 能和食盐形成食盐溶液 |
6.工业上采用氨碱法生产纯碱,主要流程如图1,请据图回答相关问题.
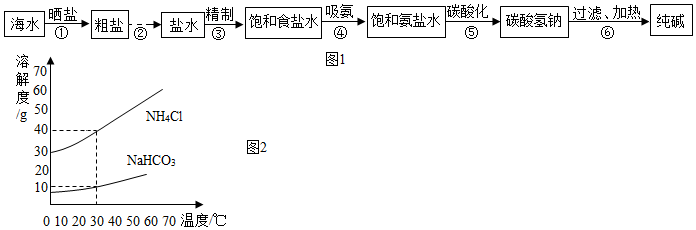
上述过程的化学原理为:NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl
(1)氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显红色.
(2)从步骤①提取粗盐常用蒸发结晶(填“蒸发结晶”或“降温结晶”)方法.
(3)氨气极易溶于水,且与水反应生成一水合氨(NH3•H2O),我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是饱和氨盐水显碱性,有利于吸收二氧化碳.
(4)氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,首先结晶析出的物质是碳酸氨钠,根据溶解度曲线(如图2)和两者的质量关系分析原因相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量.
(5)步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途治疗胃酸过多.氨碱法得到的另一产物是氯化铵,可以用作化肥中氮肥.
(6)碳酸氢钠受热易分解,除纯碱外还生成二氧化碳气体和水,步骤⑥中加热发生的化学反应方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,该反应类型属于分解反应.
(7)工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠.为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
请你据此分析计算:
①实验中产生二氧化碳的质量为6.6g;
②该产品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%).

上述过程的化学原理为:NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl
(1)氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显红色.
(2)从步骤①提取粗盐常用蒸发结晶(填“蒸发结晶”或“降温结晶”)方法.
(3)氨气极易溶于水,且与水反应生成一水合氨(NH3•H2O),我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是饱和氨盐水显碱性,有利于吸收二氧化碳.
(4)氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,首先结晶析出的物质是碳酸氨钠,根据溶解度曲线(如图2)和两者的质量关系分析原因相同条件下氯化铵的溶解度大于碳酸氢钠,并且反应生成的碳酸氢钠质量大于生成的氯化铵质量.
(5)步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途治疗胃酸过多.氨碱法得到的另一产物是氯化铵,可以用作化肥中氮肥.
(6)碳酸氢钠受热易分解,除纯碱外还生成二氧化碳气体和水,步骤⑥中加热发生的化学反应方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,该反应类型属于分解反应.
(7)工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠.为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
| 时间/s | 0 | 5 | 10 | 15 |
| 读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
①实验中产生二氧化碳的质量为6.6g;
②该产品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%).
 下列选项符合如图所示关系的是( )
下列选项符合如图所示关系的是( )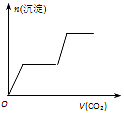



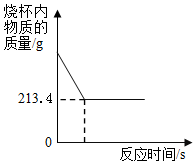 为了节约林木资源,近几年兴起了石头纸.石头纸可用沿海水产养殖中产生的大量废弃贝壳制得,为了测定某种贝壳中碳酸钙的质量分数,小明进行了以下实验:称量20.0g贝壳置于烧杯中,向其中加入200.0g稀盐酸,恰好不再产生气泡,测得的有关数据如图所示(假设贝壳中其它物质不与盐酸反应).
为了节约林木资源,近几年兴起了石头纸.石头纸可用沿海水产养殖中产生的大量废弃贝壳制得,为了测定某种贝壳中碳酸钙的质量分数,小明进行了以下实验:称量20.0g贝壳置于烧杯中,向其中加入200.0g稀盐酸,恰好不再产生气泡,测得的有关数据如图所示(假设贝壳中其它物质不与盐酸反应).